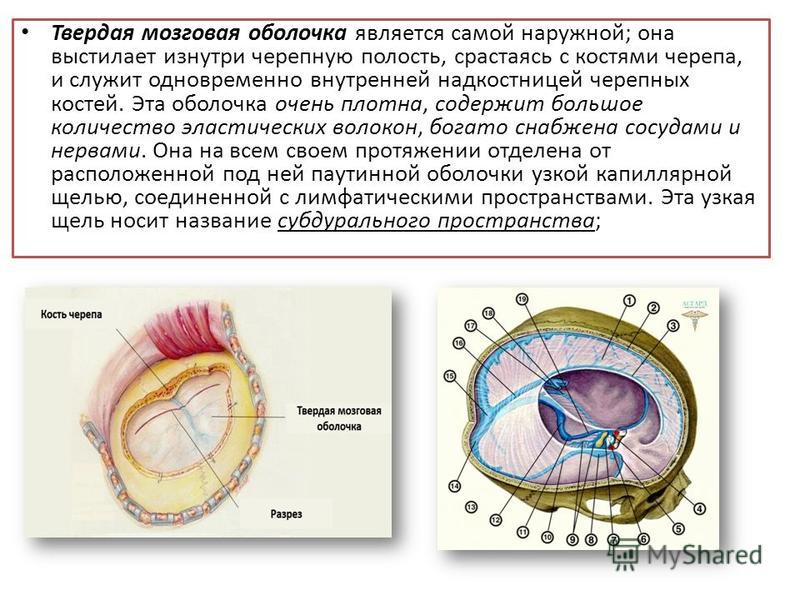
Способ герметизации швов твердой мозговой оболочки
Изобретение относится к медицине, а именно к нейрохирургии. После выполнения основного этапа операции под твердую мозговую оболочку (ТМО) на поверхность мозга укладывают пластину тахокомба с запасом по размеру на 0,5-1,0 см по всей форме раны, выступая за пределы размера разреза ТМО. Пластину тахокомба укладывают клейкой стороной, содержащей активные вещества, к ТМО, а стороной, не содержащей активных веществ, на поверхность мозга. Способ позволяет снизить послеоперационные осложнения в виде развития ликвореи, что достигается за счет укладки пластины тахокомба под ТМО и клейкой стороной к ТМО. 4 ил., 1 табл.
Изобретение относится к медицине, а именно к нейрохирургии, и может быть использовано для улучшения результатов лечения при проведении оперативных вмешательств на головном мозге.
При выполнении операций на головном мозге наиболее часто на этапе зашивания твердой мозговой оболочки (ТМО) используют простой узловой или непрерывный швы (Золтан Я.
Известено использование хирургических клеев (пат. RU № 2236260 от 10.03.2004), авторы использовали клей, состоящий из желатино-резорциновой основы, имеющей в своем составе высокомолекулярный и низкомолекулярный желатин, резорцин и дистиллированную воду, и глутарово-формальдегидного сшивающего агента, состоящего из смеси 25%-ного раствора глутарового альдегида, 40%-ного раствора формалина и дистиллированной воды в соотношении (объем.
Известны другие клеевые хирургические составы, в том числе цианакрилатные, например отечественные: МК-7М, разработчик — ВНИИИМТ; «СУЛЬФАКРИЛАТ», разработчик — Институт катализа им. Г.К. Борескова; импортные: «Ann Thorac Surgery», 1998, 66, 304-305, «J.Cardiol. Surg.», 1994, 9, 353-356; фибриновые — на основе белков, отверждаемых комплексом тромбина и хлоридом кальция; отечественные: разработки Института хирургии им. А.В. Вишневского — клей «РАБРОМ-ПАКС»; импортные: клей «ТИССУКОЛ КИТ» производства фирмы «ИММУНО АГ», Австрия; желатино-резорциновые — на основе желатина, модифицированного резорцином и сшитого глутарово-формальдегидным отвердителем; импортные: желатино-резорцино-глутарово-формальдегидный клей фирмы Fabrique d Instruments Chirurqicaux, Saint-Just-Malmont, Франция, и фирмы Nitta Gelatin, Osaka, Япония.
Клеи предназначены для различных медицинских целей, сведений о методиках применения при операциях на мозге для герметизации операционной раны твердой мозговой оболочки в уровне техники мы не обнаружили.
Наиболее близким способом герметизации шва твердой мозговой оболочки (ТМО) является применение современных клеевых композиций — например «Tissucol» (фирма Immuno, Austria) [инструкция по применению http://www.piluli.kharkov.ua/drugs/drug/tahokomb/#farm-deistvie].
Известно гемостатическое средство местного применения Тахокомб (Tachocomb), найдено в интернет https://www.rlsnet.ru/tn_index_id_3097.htm
Тахокомб следует наносить на хирургические раневые поверхности в стерильных условиях. Перед наложением губки раневая поверхность должна быть очищена от крови, дезинфицирующих и других жидкостей.
После извлечения препарата Тахокомб из внутренней стерильной упаковки губку следует смочить 0,9% раствором натрия хлорида и применить немедленно.
Сторону, покрытую активными веществами, обладающую в том числе и клеевыми свойствами, и помеченную желтым цветом, накладывают на раневую поверхность и слегка прижимают в течение 3–5 мин. Прижимание осуществляют увлажненными перчатками или увлаженной подушечкой.
Рекомендуется наносить Тахокомб на раневые поверхности исключительно в стерильных условиях во время проведения хирургического вмешательства.
Недостатком при использовании тахокомба для операций на головном мозге является чрезмерно легкое отклеивание при появлении давления ликвора изнутри после наложения на шов твердой мозговой оболочки.
Технический результат – исключение риска развития ликвореи при операциях на головном мозге, ограничение возможности попадания эпидуральной крови в субдуральное пространство в момент зашивания ТМО, минимизация риска травмы мозга инструментом в момент зашивания ТМО.
Технический результат достигают следующим образом (фиг.1). Выполняют оперативное вмешательство на головном мозге. По окончании основного этапа операции (фиг.2) перед ушиванием твердой мозговой оболочки (3) укладывают абсорбирующее гемостатическое средство для местного применения Тахокомба стороной, покрытой активными веществами (5) и обладающей клейкими свойствами, на поверхность головного мозга под твердую мозговую оболочку, к её внутренней поверхности (3) на всю длину операционной раны (2). В процессе подготовки к укладке пластину Тахокомба располагают на весу, не касаясь поверхности головного мозга (7). Пластину Тахокомба обрезают ножницами по длине и ширине так, чтобы она повторяла форму операционной раны на уровне рассеченной твердой мозговой оболочки (3), и формируют контур (8) с запасом по размеру на 0,5-1,0 см больше по всей форме раны. После этого пластину располагают клеющейся, имеющей желтый цвет (5) стороной кнаружи и подводят ее под край твердой мозговой оболочки (3) на величину сформированного запаса (8). После этого ушивают рану (фиг.4) непрерывным обвивным швом (4), достигая полной герметичности операционной раны ТМО (3).
В процессе подготовки к укладке пластину Тахокомба располагают на весу, не касаясь поверхности головного мозга (7). Пластину Тахокомба обрезают ножницами по длине и ширине так, чтобы она повторяла форму операционной раны на уровне рассеченной твердой мозговой оболочки (3), и формируют контур (8) с запасом по размеру на 0,5-1,0 см больше по всей форме раны. После этого пластину располагают клеющейся, имеющей желтый цвет (5) стороной кнаружи и подводят ее под край твердой мозговой оболочки (3) на величину сформированного запаса (8). После этого ушивают рану (фиг.4) непрерывным обвивным швом (4), достигая полной герметичности операционной раны ТМО (3).
Таким образом, предлагаемый способ герметизации швов ТМО позволяет исключить риск развития ликвореи при операциях на головном мозге. Дополнительным преимуществом методики является ограничение возможности попадания эпидуральной крови в субдуральное пространство в момент зашивания ТМО. Также предлагаемый способ позволяет минимизировать риск травмы мозга инструментом в момент зашивания ТМО.
До начала применения данной методики процент ликвореи при проведении оперативных вмешательств на головном мозге составлял более 10% в зависимости от типа операции. После начала применения данной методики с 2014 года (98 операций) число ликворей в группе высокого риска, например при операциях на задней черепной ямке, полностью устранено (см. табл.).
Таблица
Сравнительная характеристика известного и предлагаемого методов
| Показатель | Известный метод | Предлагаемый метод |
| Сроки снятия швов | 12-14 дней | 9-10 дней |
| Длительность проведения антибактериальной терапии | 10-21суток | Однократно перед операцией |
| Длительность пребывания в стационаре после операции | 12-21 день | 9-10 дней |
Клинический случай
Пациентка К. , 9 лет, госпитализирована в нейрохирургическое отделение с жалобами на эпилептические припадки, некупируемые противоэпилептическими препаратами.
, 9 лет, госпитализирована в нейрохирургическое отделение с жалобами на эпилептические припадки, некупируемые противоэпилептическими препаратами.
После проведения комплекса обследования установлен клинический диагноз: Объемное образование правого полушария головного мозга (фокальная кортикальная дисплазия), симптоматическая фармакорезистентная эпилепсия.
Показано оперативное лечение. За 30 минут до операции однократно внутримышечно введен антибактериальный препарат широкого спектра действия.
Оперирована 17.09.16 г., проведена костно-пластическая трепанация черепа справа, периинсулярная транссильвиевая функциональная гемисферотомия справа.
Протокол операции: Под эндотрахеальным наркозом, лежа на спине с поворотом головы влево из дугообразного разреза кожи в правой лобно-височно-теменной области выполнена обширная птериональная краниотомия. ТМО вскрыта основанием к птериону. Мозг изменен, атрофичен. Выполнена широкая диссекция сильвиевой щели с обнажением всей островковой доли до циркулярной борозды (верхняя и нижняя инсулярные борозды).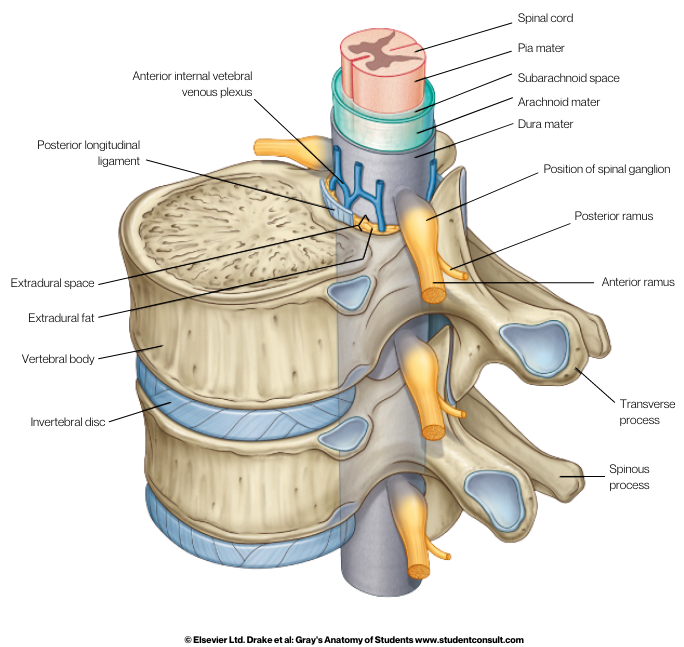
 3) не клейкой стороной на головной мозг, клейкой стороной к ТМО, затем проведено зашивание ТМО непрерывным швом (фиг.4). Кость уложена на место, фиксирована шелком и подшита по периметру трепанационного окна. Мягкие ткани послойно ушиты наглухо. Асептическая повязка.
3) не клейкой стороной на головной мозг, клейкой стороной к ТМО, затем проведено зашивание ТМО непрерывным швом (фиг.4). Кость уложена на место, фиксирована шелком и подшита по периметру трепанационного окна. Мягкие ткани послойно ушиты наглухо. Асептическая повязка.В послеоперационном периоде осложнений не отмечалось. Швы сняты на 9-й день, пациентка выписана на 10 сутки после операции.
Таким образом, нами разработан способ выполнения операций на головном мозге с использованием пластины Тахокомба иным, нежели заявлено в инструкции производителя, способом, а именно стороной, покрытой активными веществами не на поверхность раны, позволившим исключить риск развития ликвореи, ограничить возможность попадания эпидуральной крови в субдуральное пространство в момент зашивания ТМО, минимизировать риск травмы мозга инструментом в момент зашивания ТМО.
Описание к чертежам.
Фигура 1. Схема применения Тахокомба при ушивании раны после операции на головном мозге.
1 – кости черепа
2 – трепанационное окно
3 – твердая мозговая оболочка (ТМО)
4 – шов, наложенный на ТМО
5 – сторона пластины Тахокомба, покрытая активными веществами, имеющая желтый цвет
6 – не покрытая активными веществами сторона пластины Тахокомба
7 – головной мозг
Фигура 2. Вид операционной раны после завершения основного этапа операции
Вид операционной раны после завершения основного этапа операции
1 – кости черепа
3 – твердая мозговая оболочка (ТМО)
7 – головной мозг
Фигура 3. Этап укладывания пластины Тахокомба в операционную рану.
1 – кости черепа
3 – твердая мозговая оболочка (ТМО)
5 – сторона пластины Тахокомба, покрытая активными веществами, имеющая желтый цвет
8 – контур пластины Тахокомба, уложенной под ТМО – пунктирная линия
Фигура 4. ТМО ушита непрерывным обвивным швом.
1 – кости черепа
3 – твердая мозговая оболочка (ТМО)
4 – шов, наложенный на ТМО
Способ герметизации швов твердой мозговой оболочки при проведении операций на головном мозге с использованием пластины Тахокомба, отличающийся тем, что после выполнения основного этапа операции под твердую мозговую оболочку на поверхность мозга укладывают пластину Тахокомба с запасом по размеру на 0,5-1,0 см по всей форме раны, выступая за пределы размера разреза ТМО, клейкой стороной, содержащей активные вещества, к ТМО, стороной, не содержащей активных веществ, на поверхность мозга.
Способ применения при дентальной имплантации мембраны аллогенной лиофилизированной ТМО. RBB Лиопласт (Самара, Россия)
Главная → Патенты по технологии производства и применению «Лиопласт-С»® в практике → Способ применения при дентальной имплантации мембраны аллогенной ТМО
- На завершающей стадии операции края фиксированного слизисто-надкостничного покрова по периферии раны отслаиваются на 2-3 мм от линии разреза.
- Хирургическими ножницами из заготовки стерильной аллогенной лиофилизированной dura mater вырезается мембрана необходимого размера и формы.
- Подготовленная мембрана укладывается на поверхность альвеолярного отростка челюсти.
- При этом средней частью мембраны полностью перекрывается имплантат и его костное ложе.
- Периферические части мембраны располагаются на частично сошлифованной и перфорированной поверхности альвеолярного отростка.
- Края мембраны заправляются под отслоенные края слизисто-надкостничного покрова.
- Аллогенная лиофилизированная dura mater регидратируется путем смачивания кровью непосредственно в ране.
- Мембрана фиксируется путем ее прижатия слизисто-надкостничными лоскутами при наложении швов полимерной нитью на атравматической игле.
Изобретение относится к медицине и может быть использовано при дентальной имплантации. После введения дентального имплантата в подготовленное костное ложе сошлифовывают на толщину около 0,5 мм и в нескольких точках перфорируют наружную кортикальную пластинку альвеолярного отростка челюсти вокруг ложа имплантата. Отслаивают край фиксированного слизисто-надкостничного покрова по периферии раны на 2-3 мм от линии разреза. Вырезают стерильными хирургическими ножницами мембрану необходимого размеры и формы из заготовки стерильной аллогенной лиофилизированной твердой мозговой оболочки. Укладывают подготовленную мембрану на поверхность альвеолярного отростка челюсти, при этом ее средней частью полностью перекрывают имплантат в его костном ложе, периферические части мембраны укладывают на частично сошлифованную и перфорированную поверхность альвеолярного отростка, а края мембраны заправляют под отслоенные края слизисто-надкостничного покрова. Фиксируют мембрану твердой мозговой оболочки путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле и ушивают рану мягких тканей наглухо. Способ препятствует возникновению местных осложнений операции, способствует остеоинтеграции имплантата и в итоге повышает эффективность лечения.
Фиксируют мембрану твердой мозговой оболочки путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле и ушивают рану мягких тканей наглухо. Способ препятствует возникновению местных осложнений операции, способствует остеоинтеграции имплантата и в итоге повышает эффективность лечения.
Изобретение относится к медицине, а именно —к стоматологии. Способ заключается в том, что после введения дентального имплантата в подготовленное костное ложе сошлифовывают на толщину около 0,5 мм и в нескольких точках перфорируют наружную кортикальную пластинку альвеолярного отростка челюсти вокруг ложа имплантата, отслаивают край фиксированного слизисто-надкостничного покрова по периферии раны на 2-3 мм от линии разреза, вырезают стерильными хирургическими ножницами мембрану необходимого размера и формы из заготовки стерильной аллогенной лиофилизированной твердой мозговой оболочки, укладывают подготовленную мембрану на поверхность альвеолярного отростка челюсти, при этом ее средней частью полностью перекрывают имплантат в его костном ложе, периферические части мембраны укладывают на частично сошлифованную и перфорированную поверхность альвеолярного отростка, а края мембраны заправляют под отслоенные края слизисто-надкостничного покрова, после чего фиксируют мембрану твердой мозговой оболочки путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле и ушивают рану мягких тканей наглухо. Способ препятствует возникновению местных осложнений операции, способствует остеоинтеграции имплантата и в итоге повышает эффективность лечения.
Способ препятствует возникновению местных осложнений операции, способствует остеоинтеграции имплантата и в итоге повышает эффективность лечения.
Изобретение относится к медицине, в частности — к стоматологии и используется при операциях дентальной имплантации для укрытия мембраной аллогенной лиофилизированной твердой мозговой оболочки имплантата и его воспринимающего костного ложа. Известен способ использования при дентальной имплантации титановой мембраны [1], сущность которого состоит в том, что подбирают мембрану соответственно величине операционной раны, придают необходимую округлую форму при помощи хирургического инструментария, укладывают поверх имплантата, введенного в костное ложе и фиксируют к окружающей костной ткани альвеолярного отростка челюсти при помощи специальных маленьких крепежных титановых винтов. Недостатки данного способа состоят в том, что, во-первых, применение крепежных винтов усложняет технику оперативного вмешательства и вызывает дополнительное травмирование костной и мягких тканей, во-вторых, титан является нерезорбируемым материалом, вследствие чего возникает необходимость дополнительных хирургических манипуляций по извлечению мембраны. Известен способ применения политетрафторэтиленовой мембраны [2], сущность которого состоит в том, что дентальный имплантат устанавливают в альвеолу непосредственно после удаления зуба, дефект костной ткани вокруг имплантата восполняют деминерализованной лиофилизированной аллокостью либо биоабсорбируемым гидроксиапатитом, помещают мембрану из политетрафторэтилена подходящего размера на поверхность альвеолярного отростка челюсти и затем выкраивают, мобилизуют и ушивают слизисто-надкостничные лоскуты. Недостаток описанного способа заключается в том, что он не обеспечивает фиксации мембраны к костной ткани альвеолярного отростка челюсти. Кроме того, политетрафторэтиленовая мембрана, будучи не рассасываемой, требует дополнительного оперативного вмешательства для своего извлечения. Известен также способ использования при дентальной имплантации человеческой твердой мозговой оболочки [3], сущность которого заключается в том, что применяют аллогенную твердую мозговую оболочку, консервированную путем лиофилизации, толщиной от 0,25 до 0,5 мм, придают ей необходимую конфигурацию и покрывают ею альвеолярный отросток челюсти с установленным в него имплантатом, после чего ушивают рану мягких тканей.
Известен способ применения политетрафторэтиленовой мембраны [2], сущность которого состоит в том, что дентальный имплантат устанавливают в альвеолу непосредственно после удаления зуба, дефект костной ткани вокруг имплантата восполняют деминерализованной лиофилизированной аллокостью либо биоабсорбируемым гидроксиапатитом, помещают мембрану из политетрафторэтилена подходящего размера на поверхность альвеолярного отростка челюсти и затем выкраивают, мобилизуют и ушивают слизисто-надкостничные лоскуты. Недостаток описанного способа заключается в том, что он не обеспечивает фиксации мембраны к костной ткани альвеолярного отростка челюсти. Кроме того, политетрафторэтиленовая мембрана, будучи не рассасываемой, требует дополнительного оперативного вмешательства для своего извлечения. Известен также способ использования при дентальной имплантации человеческой твердой мозговой оболочки [3], сущность которого заключается в том, что применяют аллогенную твердую мозговую оболочку, консервированную путем лиофилизации, толщиной от 0,25 до 0,5 мм, придают ей необходимую конфигурацию и покрывают ею альвеолярный отросток челюсти с установленным в него имплантатом, после чего ушивают рану мягких тканей. Данный способ выбран авторами в качестве прототипа. Главный недостаток данного способа заключаются в том, что не предусмотрена должная фиксация мембраны, из-за чего возможно ее смещение относительно имплантата и нарушение герметичного укрытия костной раны. Результат, достигаемый изобретением, — уменьшение местных осложнений после операции дентальной имплантации, обеспечение благоприятных условий для полноценного сохранения или восстановления костной ткани альвеолярного отростка челюсти в зоне имплантации, создание оптимальных условий для остеоинтеграции имплантата и его долговременного функционирования. Сущность изобретения заключается в том, что после адекватного обезболивания, с учетом показаний и противопоказаний, в беззубом участке альвеолярного отростка челюсти специальным вращающим режущим инструментарием под постоянным охлаждением препарируют воспринимающее костное ложе, производят его антисептическую обработку с использованием соответствующих фармакологических препаратов и физиотерапевтических средств, устанавливают в подготовленное таким образом ложе дентальный имплантат, затем сошлифовывают на толщину около 0,5 мм и в нескольких точках перфорируют наружную кортикальную пластинку альвеолярного отростка челюсти вокруг ложа имплантата, отслаивают край фиксированного слизисто-надкостничного покрова по периферии раны на 2-3 мм от линии разреза, вырезают стерильными хирургическими ножницами мембрану необходимого размеры и формы из заготовки стерильной аллогенной лиофилизированной твердой мозговой оболочки, укладывают подготовленную мембрану на поверхность альвеолярного отростка челюсти, при этом ее средней частью полностью перекрывают имплантат в его костном ложе, периферические части мембраны укладывают на частично сошлифованную и перфорированную поверхность альвеолярного отростка, а края мембраны заправляют под отслоенные края слизисто-надкостничного покрова, после чего фиксируют мембрану твердой мозговой оболочки путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле и ушивают рану мягких тканей наглухо.
Данный способ выбран авторами в качестве прототипа. Главный недостаток данного способа заключаются в том, что не предусмотрена должная фиксация мембраны, из-за чего возможно ее смещение относительно имплантата и нарушение герметичного укрытия костной раны. Результат, достигаемый изобретением, — уменьшение местных осложнений после операции дентальной имплантации, обеспечение благоприятных условий для полноценного сохранения или восстановления костной ткани альвеолярного отростка челюсти в зоне имплантации, создание оптимальных условий для остеоинтеграции имплантата и его долговременного функционирования. Сущность изобретения заключается в том, что после адекватного обезболивания, с учетом показаний и противопоказаний, в беззубом участке альвеолярного отростка челюсти специальным вращающим режущим инструментарием под постоянным охлаждением препарируют воспринимающее костное ложе, производят его антисептическую обработку с использованием соответствующих фармакологических препаратов и физиотерапевтических средств, устанавливают в подготовленное таким образом ложе дентальный имплантат, затем сошлифовывают на толщину около 0,5 мм и в нескольких точках перфорируют наружную кортикальную пластинку альвеолярного отростка челюсти вокруг ложа имплантата, отслаивают край фиксированного слизисто-надкостничного покрова по периферии раны на 2-3 мм от линии разреза, вырезают стерильными хирургическими ножницами мембрану необходимого размеры и формы из заготовки стерильной аллогенной лиофилизированной твердой мозговой оболочки, укладывают подготовленную мембрану на поверхность альвеолярного отростка челюсти, при этом ее средней частью полностью перекрывают имплантат в его костном ложе, периферические части мембраны укладывают на частично сошлифованную и перфорированную поверхность альвеолярного отростка, а края мембраны заправляют под отслоенные края слизисто-надкостничного покрова, после чего фиксируют мембрану твердой мозговой оболочки путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле и ушивают рану мягких тканей наглухо. На практике способ осуществляется следующим образом. Проводят тщательное общее и местное обследование пациента на предмет выявления показаний и противопоказаний к дентальной имплантации с использованием аллогенных костнопластических материалов. Выполняют планирование оперативного вмешательства: рассчитывают необходимое количество дентальных имплантатов, их конструкцию, размеры и расположение в челюсти; выбирают заготовку мембраны аллогенной лиофилизированной твердой мозговой оболочки. В качестве предоперационной подготовки осуществляют исчерпывающую санацию полости рта. Непосредственно перед вмешательством больной получает премедикацию и адекватное обезболивание области операции: чаще всего местную проводниковую анестезию. В области беззубого участка альвеолярного отростка челюсти производят разрез слизистой оболочки, отслаивают и мобилизуют слизисто-надкостничный лоскут. Препарируют воспринимающее костное ложе, используя специальный режущий инструментарий, наконечник с редукцией оборотов, физиодиспенсер с регуляцией числа оборотов режущего инструмента и постоянной подачей охлаждающей жидкости.
На практике способ осуществляется следующим образом. Проводят тщательное общее и местное обследование пациента на предмет выявления показаний и противопоказаний к дентальной имплантации с использованием аллогенных костнопластических материалов. Выполняют планирование оперативного вмешательства: рассчитывают необходимое количество дентальных имплантатов, их конструкцию, размеры и расположение в челюсти; выбирают заготовку мембраны аллогенной лиофилизированной твердой мозговой оболочки. В качестве предоперационной подготовки осуществляют исчерпывающую санацию полости рта. Непосредственно перед вмешательством больной получает премедикацию и адекватное обезболивание области операции: чаще всего местную проводниковую анестезию. В области беззубого участка альвеолярного отростка челюсти производят разрез слизистой оболочки, отслаивают и мобилизуют слизисто-надкостничный лоскут. Препарируют воспринимающее костное ложе, используя специальный режущий инструментарий, наконечник с редукцией оборотов, физиодиспенсер с регуляцией числа оборотов режущего инструмента и постоянной подачей охлаждающей жидкости. Эвакуацию жидкости, слюны и крови из области операционного поля обеспечивают вакуумным хирургическим отсосом. Выполняют антисептическую обработку сформированного воспринимающего костного ложа с применением соответствующих фармакологических препаратов и физиотерапевтических средств. Устанавливают в подготовленное таким образом ложе дентальный имплантат погружной конструкции. Затем сошлифовывают на толщину около 0,5 мм и в нескольких точках перфорируют наружную кортикальную пластинку альвеолярного отростка челюсти вокруг ложа имплантата. Отслаивают край фиксированного слизисто-надкостничного покрова по периферии раны на 2-3 мм от линии разреза. Вырезают стерильными хирургическими ножницами мембрану необходимого размера и формы из заготовки стерильной аллогенной лиофилизированной твердой мозговой оболочки. Укладывают подготовленную мембрану на поверхность альвеолярного отростка челюсти, при этом ее средней частью полностью перекрывают имплантат в его костном ложе, периферические части мембраны укладывают на частично сошлифованную и перфорированную поверхность альвеолярного отростка, а края мембраны заправляют под отслоенные края слизисто-надкостничного покрова.
Эвакуацию жидкости, слюны и крови из области операционного поля обеспечивают вакуумным хирургическим отсосом. Выполняют антисептическую обработку сформированного воспринимающего костного ложа с применением соответствующих фармакологических препаратов и физиотерапевтических средств. Устанавливают в подготовленное таким образом ложе дентальный имплантат погружной конструкции. Затем сошлифовывают на толщину около 0,5 мм и в нескольких точках перфорируют наружную кортикальную пластинку альвеолярного отростка челюсти вокруг ложа имплантата. Отслаивают край фиксированного слизисто-надкостничного покрова по периферии раны на 2-3 мм от линии разреза. Вырезают стерильными хирургическими ножницами мембрану необходимого размера и формы из заготовки стерильной аллогенной лиофилизированной твердой мозговой оболочки. Укладывают подготовленную мембрану на поверхность альвеолярного отростка челюсти, при этом ее средней частью полностью перекрывают имплантат в его костном ложе, периферические части мембраны укладывают на частично сошлифованную и перфорированную поверхность альвеолярного отростка, а края мембраны заправляют под отслоенные края слизисто-надкостничного покрова. Фиксируют мембрану твердой мозговой оболочки путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле. Рану мягких тканей ушивают наглухо. В послеоперационном периоде назначают тщательную гигиеническую и антисептическую обработку полости рта, прием таблетированных антибиотиков и гипосенсибилизирующих препаратов сроком на одну неделю, а также физиотерапевтические процедуры на область оперативного вмешательства: в частности низкочастотный ультразвук и гелий-неоновый лазер. Спустя 3-6 месяцев после контрольного рентгенологического исследования, через прокол слизистой оболочки устанавливают головку имплантата и изготавливают искусственную зубную коронку с опорой на имплантат. Достоинства предлагаемого способа заключаются в следующем:
Фиксируют мембрану твердой мозговой оболочки путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле. Рану мягких тканей ушивают наглухо. В послеоперационном периоде назначают тщательную гигиеническую и антисептическую обработку полости рта, прием таблетированных антибиотиков и гипосенсибилизирующих препаратов сроком на одну неделю, а также физиотерапевтические процедуры на область оперативного вмешательства: в частности низкочастотный ультразвук и гелий-неоновый лазер. Спустя 3-6 месяцев после контрольного рентгенологического исследования, через прокол слизистой оболочки устанавливают головку имплантата и изготавливают искусственную зубную коронку с опорой на имплантат. Достоинства предлагаемого способа заключаются в следующем:
- используют мембрану аллогенной лиофилизированной твердой мозговой оболочки, которая является костнопластическим, остеоиндуктивным материалом, то есть оказывает активизирующее влияние на процессы репаративного остеогенеза, что способствует сохранению или восстановлению объема и плотности костной ткани беззубого участка альвеолярного отростка и содействует достижению остеоинтеграции имплантата;
- придают мембране необходимые размер и форму непосредственно во время оперативного вмешательства посредством вырезания из заранее выбранной стерильной заготовки, что удобно для работы оперирующего хирурга и позволяет достичь должной точности;
- мембрану аллогенной лиофилизированной твердой мозговой оболочки укладывают на поверхность альвеолярного отростка и укрывают ею дентальный имплантат и его костное ложе, что препятствует проникновению в костную рану инфекции со стороны полости рта и, следовательно, способствует уменьшению местных воспалительных осложнений после операции дентальной имплантации;
- мембрану аллогенной лиофилизированной твердой мозговой оболочки накладывают между костной тканью альвеолярного отростка и слизисто-надкостничным покровом, что предотвращает врастание в костную рану эпителия и тем самым создает благоприятные условия для остеоинтеграции имплантата;
- частично сошлифовывают и перфорируют наружную кортикальную пластинку альвеолярного отростка, что, во-первых, способствует более интимному слиянию мембраны с костной тканью челюсти и улучшает ее барьерные функции, во-вторых, вмешательство на кортикальной пластинки альвеолы вызывает активизацию собственных местных факторов репаративного остеогенеза, вследствие чего улучшаются условия для сохранения или восстановления объема и плотности костной ткани беззубого участка альвеолярного отростка и достижения остеоинтеграции имплантата;
- отслаивают край фиксированного слизисто-надкостничного покрова по периферии раны на 2-3 мм от линии разреза, заправляют под него края мембраны твердой мозговой оболочки, фиксируют мембрану путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле, что обеспечивает надежное удержание мембраны в заданном положении.
Источники информации1. Мушеев И.У., Олесова В.Н., Фрамович О.3. Практическая дентальная имплантология. — М.: Парадиз, 2000. — С.197-201.2. Becker W., Becker B.E. Guided tissue regeneration for implants placed into extraction sockets and for implant dehiscences: Surgical technique and case reports. // Int. J. Periodontics Restorative Dent. — 1990. — Vol.10. — P.377-391.3. Peleg M., Chaushu G., Blinder D., Taicher S. Use of Lyodura for Bone Augmentation of Osseous Defects Around Dental Implants. // J. Periodontol. — 1999. — Vol.70. — P.853-860.
Формула изобретения
Способ применения мембраны аллогенной лиофилизированной твердой мозговой оболочки при дентальной имплантации, заключается в том, что производят соответствующую инструментальную и антисептическую подготовку воспринимающего костного ложа в беззубом участке альвеолярного отростка челюсти, устанавливают в него дентальный имплантат, альвеолярный отросток в зоне имплантации укрывают мембраной аллогенной лиофилизированной твердой мозговой оболочки и ушивают рану мягких тканей, отличающийся тем, что после введения дентального имплантата и перед наложением мембраны сошлифовывают на толщину около 0,5 мм и в нескольких точках перфорируют наружную кортикальную пластинку альвеолярного отростка челюсти вокруг ложа имплантата, отслаивают край фиксированного слизисто-надкостничного покрова по периферии раны на 2-3 мм от линии разреза, вырезают стерильными хирургическими ножницами мембрану необходимого размеры и формы из заготовки стерильной аллогенной лиофилизированной твердой мозговой оболочки, укладывают подготовленную мембрану на поверхность альвеолярного отростка челюсти, при этом средней частью мембраны полностью перекрывают имплантат и его костное ложе, периферические части мембраны укладывают на частично сошлифованную и перфорированную поверхность альвеолярного отростка, а края мембраны заправляют под отслоенные края слизисто-надкостничного покрова, после чего фиксируют мембрану твердой мозговой оболочки путем наложения швов к краям слизистой оболочки при помощи полимерной нити на атравматической игле.
Онтология и база знаний трансляционной медицины: развитие персонализированной медицины путем преодоления разрыва между лабораторным и прикроватным лечением
. 2011 г., 17 мая; 2 Приложение 2 (Приложение 2): S1.
дои: 10.1186/2041-1480-2-S2-S1.
Джоан С Лучано 1 , Боссе Андерссон, Колин Бэтчелор, Оливье Боденрейдер, Тим Кларк, Кристин К. Денни, Кристофер Домарью, Томас Гамбет, Ли Харланд, Аня Дженч, Випул Кашьяп, Питер Кос, Джулия Козловски, Тимоти Лебо, Скотт М. Маршалл, Джейми П. МакКаскер
Принадлежности
принадлежность
- 1 Политехнический институт Ренсселера, г. Трой, штат Нью-Йорк, США. [email protected].
- PMID: 21624155
- PMCID: PMC3102889
- DOI:
10.
 1186/2041-1480-2-С2-С1
1186/2041-1480-2-С2-С1
Бесплатная статья ЧВК
Джоанн С. Лучано и др. Дж. Биомедицинская семантика. .
Бесплатная статья ЧВК
. 2011 г., 17 мая; 2 Приложение 2 (Приложение 2): S1.
дои: 10.1186/2041-1480-2-S2-S1.
Авторы
Джоан С Лучано 1 , Боссе Андерссон, Колин Бэтчелор, Оливье Боденрейдер, Тим Кларк, Кристин К. Денни, Кристофер Домарью, Томас Гамбет, Ли Харланд, Аня Дженч, Випул Кашьяп, Питер Кос, Джулия Козловски, Тимоти Лебо, Скотт М. Маршалл, Джейми П. МакКаскер
принадлежность
- 1 Политехнический институт Ренсселера, г.
 Трой, штат Нью-Йорк, США. [email protected].
Трой, штат Нью-Йорк, США. [email protected].
- PMID: 21624155
- PMCID: PMC3102889
- DOI: 10.1186/2041-1480-2-С2-С1
Абстрактный
Фон: Трансляционная медицина требует интеграции знаний с использованием разнородных данных от здравоохранения до наук о жизни. Здесь мы описываем совместные усилия по созданию прототипа базы знаний по трансляционной медицине (TMKB), способной отвечать на вопросы, касающиеся клинической практики и открытия фармацевтических препаратов.
Полученные результаты: Мы разработали Онтологию трансляционной медицины (TMO) как объединяющую онтологию для интеграции химических, геномных и протеомных данных с данными о заболеваниях, лечении и электронными медицинскими картами. Мы демонстрируем использование технологий Semantic Web для интеграции данных о пациентах и биомедицинских данных и показываем, как такая база знаний может помочь врачам в обеспечении индивидуального ухода за пациентами и облегчении набора пациентов для участия в активных клинических испытаниях. Таким образом, пациенты, врачи и исследователи могут изучить базу знаний, чтобы лучше понять терапевтические возможности, эффективность и механизмы действия.
Мы демонстрируем использование технологий Semantic Web для интеграции данных о пациентах и биомедицинских данных и показываем, как такая база знаний может помочь врачам в обеспечении индивидуального ухода за пациентами и облегчении набора пациентов для участия в активных клинических испытаниях. Таким образом, пациенты, врачи и исследователи могут изучить базу знаний, чтобы лучше понять терапевтические возможности, эффективность и механизмы действия.
Выводы: Эта работа является важным шагом в использовании технологий Semantic Web для облегчения интеграции соответствующих распределенных внешних источников и продвижения к вычислительной платформе для поддержки персонализированной медицины.
Доступность: TMO можно загрузить с http://code.google.com/p/translationalmedicineontology, а TMKB можно получить по адресу http://tm.semanticscience. org/sparql.
org/sparql.
Цифры
Рисунок 1
Обзор TMO. Обзор выбранных…
Рисунок 1
Обзор TMO. Обзор выбранных типов, подтипов (перекрытие) и экзистенциальных ограничений (стрелки) в…
Рисунок 1Обзор ТМО. Обзор отдельных типов, подтипов (перекрытие) и экзистенциальных ограничений (стрелки) в онтологии трансляционной медицины.
Рисунок 2
Запрос №1: Побочные эффекты. …
Рисунок 2
Запрос №1: Побочные эффекты. Элементы данных, задействованные в запросе №1. Вопрос…
Элементы данных, задействованные в запросе №1. Вопрос…
Запрос №1: Побочные эффекты. Элементы данных, задействованные в запросе №1. Запрос можно сформулировать так: «Сколько пациентов испытывали побочные эффекты при приеме донепезила?»
Рисунок 3
Обзор ТКМБ. Обзор…
Рисунок 3
Обзор ТКМБ. Обзор содержимого Базы знаний трансляционной медицины (TMKB).…
Рисунок 3 Обзор ТКМБ. Обзор содержимого Базы знаний трансляционной медицины (TMKB). TMKB состоит из онтологии трансляционной медицины с сопоставлениями с онтологиями и терминологиями, перечисленными на биопортале NCBO. TMO предоставляет глобальную схему для электронных медицинских карт (EHR) на основе Indivo и может использоваться с формализованными критериями болезни Альцгеймера. Типы карт TMO из источников Linking Open Data.
Типы карт TMO из источников Linking Open Data.
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Вычислительная структура для поддержки интеграции биомолекулярных и клинических данных в рамках трансляционного подхода.
Миёси Н.С., Пинейро Д.Г., Сильва В.А. младший, Фелипе Дж.К. Миёси Н.С. и соавт. Биоинформатика BMC. 2013 6 июня; 14:180. дои: 10.1186/1471-2105-14-180. Биоинформатика BMC. 2013. PMID: 23742129Бесплатная статья ЧВК.
OpenFlyData: образцовая сеть данных, объединяющая данные об экспрессии генов плодовой мушки Drosophila melanogaster.
Майлз А., Чжао Дж., Клайн Г., Уайт-Купер Х., Шоттон Д. Майлз А.
 и др.
Дж. Биомед Информ. 2010 окт; 43 (5): 752-61. doi: 10.1016/j.jbi.2010.04.004.
Дж. Биомед Информ. 2010.
PMID: 20382263
и др.
Дж. Биомед Информ. 2010 окт; 43 (5): 752-61. doi: 10.1016/j.jbi.2010.04.004.
Дж. Биомед Информ. 2010.
PMID: 20382263Когнитивные ИТ-системы для анализа больших данных в медицине.
Исакова Ж. Исакова Ю. Int J Risk Safe Med. 2015;27 Приложение 1:S108-9. DOI: 10.3233/JRS-150711. Int J Risk Safe Med. 2015. PMID: 26639685
Семантическая сеть в трансляционной медицине: текущие приложения и будущие направления.
Мачадо К.М., Ребхольц-Шуманн Д., Фрейтас А.Т., Коуто FM. Мачадо CM и соавт. Кратко Биоинформ. 2015 янв;16(1):89-103. дои: 10.1093/bib/bbt079. Epub 2013 6 ноября. Кратко Биоинформ. 2015. PMID: 24197933 Бесплатная статья ЧВК. Обзор.

Семантически включение фармакогеномных данных для реализации персонализированной медицины.
Самвальд М., Куле А., Уэрга И., Пауэрс Р.Л., Лучано Дж.С., Фреймут Р.Р., Уиппл Ф., Пихлер Э., Прюдоммо Э., Дюмонтье М., Маршалл М.С. Самвальд М. и соавт. Фармакогеномика. 2012 Январь; 13 (2): 201-12. дои: 10.2217/стр.11.179. Фармакогеномика. 2012. PMID: 22256869 Бесплатная статья ЧВК. Обзор.
Посмотреть все похожие статьи
Цитируется
На пути к фундаментальному представлению потенциальных знаний о взаимодействии наркотиков.
Броххаузен М., Шнайдер Дж., Мэлоун Д., Эмпи П.Е., Хоган В.Р., Бойс Р.Д. Броххаузен М. и соавт.
 Протокол семинара CEUR. 2014 окт;1309: 16-31.
Протокол семинара CEUR. 2014.
PMID: 33139970
Бесплатная статья ЧВК.
Протокол семинара CEUR. 2014 окт;1309: 16-31.
Протокол семинара CEUR. 2014.
PMID: 33139970
Бесплатная статья ЧВК.Фрагменты текста для подтверждения медицинских отношений: неконтролируемый подход с использованием диаграммы знаний и вложений.
Камдар М.Р., Стэнли К.Э., Кэрролл М., Вогулис Л., Доулинг В., Деус Х.Ф., Самарасингхе М. Камдар М.Р. и соавт. AMIA Jt Summits Transl Sci Proc. 2020 30 мая; 2020: 288-297. Электронная коллекция 2020. AMIA Jt Summits Transl Sci Proc. 2020. PMID: 32477648 Бесплатная статья ЧВК.
Агрономические связанные данные (AgroLD): система, основанная на знаниях, позволяющая использовать интегративную биологию в агрономии.
Венкатесан А., Тагни Нгомпе Г.
 , Хассуни Н.Э., Чентли И., Гиньон В., Жонке С., Руис М., Ларманд П.
Венкатесан А. и соавт.
ПЛОС Один. 30 ноября 2018 г .; 13 (11): e0198270. doi: 10.1371/journal.pone.0198270. Электронная коллекция 2018.
ПЛОС Один. 2018.
PMID: 30500839
Бесплатная статья ЧВК.
, Хассуни Н.Э., Чентли И., Гиньон В., Жонке С., Руис М., Ларманд П.
Венкатесан А. и соавт.
ПЛОС Один. 30 ноября 2018 г .; 13 (11): e0198270. doi: 10.1371/journal.pone.0198270. Электронная коллекция 2018.
ПЛОС Один. 2018.
PMID: 30500839
Бесплатная статья ЧВК.Обнаружение связи между UMLS и DBPedia посредством кругового разрешения.
Куццола Дж., Багери Э., Йованович Дж. Куццола Дж. и др. J Am Med Inform Assoc. 2018 1 июля; 25 (7): 819-826. doi: 10.1093/jamia/ocy021. J Am Med Inform Assoc. 2018. PMID: 29648604 Бесплатная статья ЧВК.
Предикатно-ориентированный анализ шаблонов для обнаружения биомедицинских знаний.
Шэнь Ф., Лю Х., Сон С., Ларсон Д.В.
 , Ли Ю.
Шен Ф. и др.
Intel Inf Manag. 2016 май;8(3):66-85. doi: 10.4236/iim.2016.83006.
Intel Inf Manag. 2016.
PMID: 28983419
Бесплатная статья ЧВК.
, Ли Ю.
Шен Ф. и др.
Intel Inf Manag. 2016 май;8(3):66-85. doi: 10.4236/iim.2016.83006.
Intel Inf Manag. 2016.
PMID: 28983419
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Грантовая поддержка
- R01 LM010130/LM/NLM NIH HHS/США
- R01 LM011566/LM/NLM NIH HHS/США
- Z99 LM999999/ImNIH/Intramural NIH HHS/США
Что означает медицинская аббревиатура ТМО?
В науке и медицине онтология трансляционной медицины расшифровывается как медицинская аббревиатура TMO.
| AADS | Противоаритмические препараты |
| AAEM | Американская академия скорой медицинской помощи |
| APRL | Archaeological Preservation Research Laboratory |
| APVMA | American Pre Veterinary Medical Association |
| ARB | Angiotensin Receptor Blocker |
| ASAT | Aspartate Aminotransferase |
| BWMF | Burma Женский медицинский фонд |
| C-B | грудь-спина |
| CBD | Общий желчный проток; Дренаж закрытого мешка |
| CERH | Center for Environmental and Respiratory Health |
| CIPN | Chemotherapy-Induced Peripheral Neuropathy |
| CMER | Center for Medical Education and Research |
| CPC | clinicopathologic conference |
| CRT-P | Сердечная ресинхронизирующая терапия Кардиостимулятор |
| DHCC | Комиссия по здравоохранению штата Делавэр |
| DHEAS | dehydroepiandrosterone sulfate |
| EDP | erythema dyschromicum perstans |
| EOGD | E Octocarinatus Genome Database |
| FLM | Free Little Medicine |
| FNP | family nurse practitioner |
| GAB | Группа генетических алгоритмов |
| GIG | Группа непереносимости глютена |
| GMR | Gallups, Murmurs, Rubs |
| Gln | glutamine |
| HCGM | Helmsley Center for Genomic Medicine |
| HD | Hemodialysis |
| HDFN | Human Dermal Fibroblasts неонатальный |
| HGRC | Комитет по пересмотру руководящих принципов здравоохранения |
| HPFA | Фонд укрепления здоровья для всех |
| HRH | Hendricks Regional Health |
| HSG | гистеросальпингограмма; herpes simplex, genitalis |
| HUG | Health Users Group |
| HemOnc | hematology/oncology |
| ICMS | International Congress of Medical Sciences |
| IDBS | Implant Dentistry Basic Start-up kit |
| IJML | Международный журнал медицинской лаборатории |
| IMN | International Medical Network |
| IPAC | Infection Prevention And Control |
| JNHS | Japan Nurses Health Study |
| KHV | Koi Herpes Virus |
| LGSIL | low Плоскоклеточное внутриэпителиальное поражение средней степени |
| LTD | минимальная переносимая доза |
| ИМАО | ингибитор моноаминоксидазы |
| MCC | серьезное осложнение или сопутствующее заболевание; motorcycle collision |
| MERT | medical emergency response team |
| MIMM | Medical Marijuana In Massachusetts |
| MSES | Medical Staff Engagement Society |
| MVA | motor vehicle accident |
| NB | новорожденный |
| NCP | План сестринского ухода |
| NHLP | National Health Law and Policy |
| NP-CPAP | nasopharyngeal continuous positive airway pressure |
| NVR | Neovascularization of the retina |
| ONSD | Optic Nerve Sheath Диаметр |
| ОАС | Обструктивное апноэ во сне |
| PBSC | Стволовые клетки периферической крови |
| PCIS | Post-Cardiac Injury Syndrome |
| PCORI | Patient-Centered Outcomes Research Institute |
| PIMP | Party of Important Male Physicians |
| QMUR | QualMed Utilization Review |
| RA | Правое предсердие |
| RAA | ренин-ангиотензин-альдостерон (система) |
| RACMA | Королевский Австралазийский колледж медицинских администраторов |
| RMHU | Отдел психического здоровья жилого здоровья |
| ROM | . |