Жидкий раствор — Циклопедия
Химия для чайников. Лекция 37. Растворы // Телеканал Первый образовательныйЖидкий раствор — раствор веществ в жидкой агрегатной фазе.
Жидкие растворы, как и жидкие вещества, обладают внутренней структурой ближнего порядка. При этом структура разбавленных растворов ближе к структуре растворителя, а концентрированных — к структуре растворенного вещества.
[править] Сольваты и гидраты
Комплексные соединения, в которых частицы растворенного вещества связаны с частицами растворителя, называются сольватами, а если растворитель — вода, то гидратами.
Основу теории жидких растворов как сольватов заложил Дмитрий Иванович Менделеев.
Распад вещества на сольватированные ионы под действием молекул растворителя называется ионизацией вещества в растворах или электролитической диссоциацией.
Распад на ионы связан либо с явлением диссоциации (разъединения), либо с явлением ионизации (образования ионов). Так, при растворении ионных соединений (поскольку они уже состоят из ионов) имеет место диссоциация. Роль растворителя в этом случае заключается в создании условий для разъединения ионов противоположного знака и в препятствовании процессу молизации. Диссоциация ионных соединений протекает тем легче, чем полярнее молекулы растворителя.
При распаде ковалентных соединений на ионы происходит гетеролитический разрыв связи, т.е. ионизация. Каждое вещество в данном растворителе и при данных условиях характеризуется определенной степенью ионизации(отношение числа молей ионизированного вещества к общему числу молей растворенного).
Наиболее сильно ионизирующими растворителями являются вода, жидкие аммиак и фторид водорода (потому что диполи и потому что образуют водородную связь).
Последующее взаимодействие между частицами растворенного вещества и растворителя называется сольватацией. В результате сольватации образуются сольватированные комплексы (сольваты), в водных растворах — гидратированные аквакомплексы. Образование катионных аквакомплексов обычно объясняется донорно-акцепторным взаимодействием катиона с молекулами воды, а анионных аквакомплексов — водородной связью.
Координационное число центральных ионов в аквакомплексах в разбавленных растворах (т.е. при достаточном количестве молекул воды) в общем случае соответствует значению характерного координационного числа катиона (акцептора) и аниона (донора).
[править] Виды сольватации
Время жизни сольватов определяется характером и интенсивностью межмолекулярных взаимодействий, но обычно очень маленькое из-за обмена частицами в сольватной оболочке. В соответствии с типами межмолекулярного взаимодействия выделяют неспецифическую и специфическую сольватацию.
[править] Энергетический эффект образования жидкого раствора
При растворении разрушается связь между частицами растворяемого вещества, что связано с затратой энергии. В то же время протекает процесс сольватации, который сопровождается, наоборот, выделением энергии. Общий баланс может быть и положительным, и отрицательным.
При растворении газов и жидкостей теплота обычно выделяется. В частности, с выделением теплоты протекает смешение воды и спирта. При растворении в воде твердых веществ теплота может и выделяться и поглощаться, поэтому нагревание может как способствовать растворимости, так и препятствовать. Если растворение вещества сопровождается выделением теплоты, то при нагревании его растворимость падает. Если же вещества растворяются с поглощением теплоты, то нагревание вызывает увеличение растворимости. Зависимость растворимости в воде от температуры обычно известна экспериментально и сообщается в справочниках табличным способом.
При растворении происходят также и другие процессы, такие как изменение объема, окраски и других свойств раствора по сравнению со свойствами входящих в него веществ, поэтому с определенной точки зрения растворы являются переходным звеном между химическими веществами и смесями.
При растворении нелетучего вещества температура кипения раствора повышается по сравнению с растворителем, а температура замерзания снижается.
Исследование свойств разбавленных растворов неэлектролитов показало, что понижение давления пара, повышение температуры кипения и понижение температуры замерзания обусловлены только числом растворенных частиц в определенном объеме данного растворителя и не зависят от природы растворенного вещества. Зависимость изменений температур кипения и замерзания от концентрации описывают законы Рауля, согласно которым изменения в температурах кипения и замерзания прямо пропорциональны молярной концентрации растворенного вещества.
Пусть разность между температурой кристаллизации растворителя T°fr и температурой начала кристаллизации раствора Tfr, m — молярная концентрация, тогда:
- [math]T_{fr}^o — T_{fr} = \Delta T_{fr} = Km[/math]
Аналогично и для температуры замерзания.
Коэффициенты пропорциональности, зависящие от природы растворителя, называют криоскопической (для температуры замерзания) и эбулиоскопической (для температуры кипения) константами. Для воды криоскопическая константа равна 1.86, эбулиоскопическая равна 0.52.
Если вместо молярной концентрации в формулу подставить ее выражение через массу и молярную массу (M/m), то можно по изменению температуры кипения подсчитывать молярную массу растворенного вещества, что позволяет определить это вещество.
Для растворов электролитов изменения температур кипения и замерзания всегда больше вычисленных по законам Рауля, что объясняется ионизацией электролита (данный факт лежит в основе теории ионизации).
cyclowiki.org
Растворы
Растворами называются термодинамически устойчивые гомогенные системы, состоящие из двух и более веществ, а также продуктов их взаимодействия между собой.
Вещества, образующие раствор, называются иначе его компонентами.Их состав и концентрация в растворе могут изменяться в пределах ограниченных взаимной растворимостью.
Характерной особенностью растворов является то, что составляющие их компоненты присутствуют в них в виде отдельных молекул или ионов, которые равномерно распределяются по всему объему системы. В связи с этим в растворах отсутствует поверхность раздела между веществами и не протекают поверхностные явления, приводящие к значительному увеличению внутренней энергии. Такие растворы называются иначе истинными. Они являются термодинамически устойчивыми, образуются самопроизвольно и могут существовать неограниченно долгое время, если не изменять их количественный состав и условия хранения.
Истинные растворы в зависимости от своего агрегатного состояния подразделяются на газообразные, твердые и жидкие.
Газообразные растворыназываются иначе газовыми смесями. Примером такой смеси может служить земная атмосфера, состоящая, главным образом, из азота и кислорода, а также некоторых других веществ, присутствующих в значительно меньших количествах (углекислого газа, водяных паров, благородных газов и т.д.).
Твердыми растворамиявляются многие сплавы металлов, некоторые неорганические минералы. Образуются твердые растворы при кристаллизации расплавов.
Наибольшее распространение в природе и в хозяйственной деятельности человека получили жидкие растворы.Они, в свою очередь, подразделяются на растворы газов в жидкостях, жидкостей в жидкостях и растворы твердых веществ в жидкостях.
Различают также растворы низкомолекулярных соединений (НМС) и растворы высокомолекулярных соединений (ВМС). Последние по многим свойствам значительно отличаются от растворов НМС и поэтому будут рассмотрены отдельно.
При характеристике составных частей жидких растворов используют понятия растворительирастворенное вещество. Однако, провести между ними четкую разграничительную линию удается не всегда. Легче всего это сделать, если образующие раствор вещества, в индивидуальном виде находятся в разных агрегатных состояниях. В этом случае растворителем всегда считается то вещество, которое при тех же условиях, что и получившийся раствор, является жидкостью. Твердые и газообразные вещества, входящие в состав такого раствора, называются растворенными веществами.
При образовании раствора из двух смешивающихся жидкостей растворителем чаще всего называют то вещество, которое присутствует в растворе в бóльших количествах, или же по взаимной договоренности какое-то конкретное вещество (например, Н2О), независимо от его содержания в системе.
К твердым растворам и газовым смесям понятия растворитель и растворенное вещество не применяют.
Жидкие растворы, в которых в качестве растворителя выступает Н2О, называютсяводными. Если растворителем является какая-то другая жидкость –неводными.
Для медицины наибольшее значение имеют водные растворы, т.к. Н2О является универсальным растворителем для веществ самой различной природы и составляет основную часть внутренней среды человеческого организма. В зависимости от возраста человека на долю воды в его теле может приходиться от 80 до 50% по массе. При этом важнейшие биологические жидкости (кровь, лимфа, моча, слюна, пот и т.д.) содержат в своем составе различные растворенные вещества: неорганические соли, белки, углеводы, аминокислоты и другие гетеро- и полифункциональные органические соединения. В водной среде в живых организмах протекают многочисленные биохимические реакции. Усваивание пищи связано с переходом питательных веществ в растворенное состояние. Это облегчает их дальнейшую транспортировку биологическими жидкостями к органам и тканям. Выведение из организма метаболитов также осуществляется путем перевода их в растворенное состояние.
studfiles.net
Растворы жидкие, вещество растворенное — Справочник химика 21
Спектрофотометр СФД-2 (СФД-2 м). Спектрофотометр СФД-2 предназначен для изучения спектров поглощения жидких веществ, растворов и веществ в твердом состоянии в области спектра от 220 до 1000 нм. В приборе установлено два источника излучения — во- [c.40]Классификация двухкомпонентных растворов летучих жидких веществ. Основные признаки идеальных и предельно разбавленных растворов. Жидкие вещества при обычных условиях могут смешиваться друг с другом в любых соотношениях или ограниченно. В данной главе преимущественно будут рассмотрены законы равновесия между жидкой и паровой фазами систем, образованных двумя достаточно летучими и неограниченно растворимыми друг в друге компонентами. Раствор ацетона в воде-—пример подобной двойной (бинарно й 1 ж и д к о й системы. [c.179]
То же произойдет при прибавлении жидкости А к В. При образуется раствор жидкого вещества В, насыщенного А. Совокупность точек, отвечающих [c.170]
Выше отмечалось, что измерение диэлектрической проницаемости жидких веществ (растворов электролитов), обладающих высокой электропроводностью ( >10— сим-см- , затруднительно вследствие малой величины токов смещения по сравнению с токами проводимости. Изменить это соотношение в пользу токов смещения можно, повышая рабочую частоту переменного напряжения до частот порядка 10 —10″ гц (так называемые дециметровые или сантиметровые волны).
Таким образом, полярность молекул растворителя имеет важное значение и показывает, что чем больше их дипольный момент (и, следовательно, выше диэлектрическая проницаемость), тем выше их способность сольватировать, тем больше выделяется энергии и лучше идет растворение. С другой стороны, способность твердых и жидких веществ растворяться также в значительной мере зависит от полярности их собственных молекул. Хорошая растворимость, например, сахаров, не образующих ионов, обусловлена присутствием в их молекулах многочисленных полярных спиртовых групп. [c.16]
Примечание. I — насыщенный раствор в присутствии твердого или жидкого вещества — раствор, насыщенный газом при давлении 1 атм. [c.14]
При возбуждении люминесценции в каждом конкретном случае следует разумно подходить к выбору источника возбуждения. Для возбуждения люминесценции жидких веществ (растворов) целесообразнее всего использовать УФ- и видимый свет. Люминесценцию твердых веществ, например кристаллофосфоров, можно возбуждать УФ- или видимым светом, рентгеновскими и катодными лучами. В дальнейшем мы будем рассматри- [c.498]
Недостатки распылительной сушки — большие габариты сушильной камеры и рукавного фильтра (см. гл. 2), улавливающего наиболее мелкую пыль, уносимую из сушилки потоком теплоносителя удельные расходы сушильного агента и теплоты при распылительной сушке оказываются значительными. С другой стороны, это, по существу, единственный способ сушки жидких веществ (растворов, суспензий и т. п.), поскольку сушка жидкостей в камерных сушилках хоть и является принципиально возможной, но показатели процесса при этом хуже, а процесс сушки в псевдоожиженном слое не обладает желательной устойчивостью, что часто приводит к образованию агломератов влажного материала.
Водные растворы жидких веществ, преимущественно органических, в лабораториях готовят не так часто. Важнейшими жидкостями, растворы которых иногда приходится готовить, являются метиловый и этиловый спирты, ацетон и некоторые другие. [c.311]
Физическое состояние веи ества и природа растворителя. Для данного соединения частота колебания зависит от того, находится ли оно в чистом виде (газообразном, жидком или твердом состоянии) или в растворе. Если вещество растворено, то частота колебаний зависит от природы растворителя. Например, валентные колебания СО-группы амидов в разбавленных растворах имеют волновое число около 1690 см , а в твердом состоянии соответствующее поглощение происходит вблизи 1650 слг . Подобным образом волновое число валентных колебаний СО-группы в парах метилацетата равно 1774 см . Для этого же соединения, растворенного в циклогексане, оно равно 1756 в диоксане— 1747 и в бромоформе—1738 см . Такие различия в частотах колебаний, конечно, обусловлены влиянием различий в межмолекулярных взаимодействиях между поглощающими излучение молекулами, находящимися в твердом состоянии, и между взаимодействием этих молекул с молекулами растворителя в случае раствора. (Если колеблющуюся молекулу можно рассматривать как колеблющийся диполь и если взаимодействие исследуемых молекул с молекулами растворителя является просто диполь-диполь-ным взаимодействием, то между частотой и диэлектрической постоянной растворителя имеется простое теоретическое соотношение. Это соотношение применимо в случае некоторых, но ни в коем случае не всех эффектов, обусловленных растворителем . ) [c.96]
Жидкие вещества растворяются в воде по-разному. Винный спирт, серная кислота, азотная кислота растворяются в воде очень хорошо. Некоторые жидкости (масло, бензин, керосин) в воде не растворяются. [c.46]
Приготовление стандартного раствора жидкого вещества. Вещество, предназначенное для приготовления стандартного раствора, предварительно перегоняют. Берут фракцию, отвечающую по точке кипения искомому веществу. В некоторых случаях стандартный раствор готовят из вещества, применяемого на производстве, без перегонки.
Любой раствор состоит из растворителя и растворенного вещества. Обычно растворителем называют вещество, которое образует среду для растворенного вещества и которое в чистом виде находится в том же агрегатном состоянии, что и раствор. Так, если в жидком веществе растворено твердое или газообразное, то растворителем будет жидкость, а твердое и газообразное будут растворенными веществами. [c.145]
По отношению к жидкой дисперсионной среде коллоидные растворы делятся на две основные группы. К первой относятся главным образом растворы неорганических веществ (растворы металлов золота, серебра и др.), гидроокиси железа, многие сульфиды металлов, некоторые золи органических веществ (гидрозоль парафина, мастики и др.). Эти коллоидные растворы гетерогенные, высокодисперсные, характеризуются высокой чувствительностью к электролиту, под влиянием которого легко коагулируют и обратно в раствор не переходят (необратимые коллоиды) вязкость их близка к вязкости истинных растворов. Не проявляют сродства к дисперсионной среде и практически в ней нерастворимы, образуют микрогетерогенные системы. Относительная устойчивость их обусловливается одинаковым (положительным или отрицательным) электрическим зарядом коллоидных частиц. [c.289]
Направление научных исследований применение химической продукции в строительстве химические добавки, улучшающие свойства бетона и цементных растворов жидкие цементные растворы и материалы для покрытия полов красящие вещества для бетона разнообразные покрытия, укрепляющие поверхность химические отвердители химические вещества, защищающие бетон от воздействия воды. [c.143]
Жидкость закипает, когда давление ее насыщенного пара становится равным внешнему давлению (см. рис. 137). При уменьшении внешнего давления уменьшается и температура кипения жидкости. Если внешнее давление не изменяется и жидкость не содержит примесей,то температура кипения в процессе перегонки не изменяется. При перегонке растворов жидких веществ температура кипения постепенно повышается к концу процесса [c.305]
Спектрофотометр СФ-16. Спектрофотометр СФ-16 предназначен для изучения спектров поглощения твердых, жидких веществ растворов в области спектра 185—1100 нм. Принцип устройства и оптическая схема спектрофотометра СФ-16 не отличаются от СФ-4. Отличие заключается лишь в том, что в спектрофотометре, СФ-16 вместо водородной установлена дейтериевая лампа, обеспечивающая работу в диапазоне длин волн 185—200 нм. При работе в области длин волн от 185 до 200 нм необходимо работать в атмосфере азота. [c.42]
Разведение жидких веществ (растворов, эссенций, тинктур) проводят в помещении, защищенном от непосредственного солнечного света. Используемые для этих целей склянки должны иметь объем на 1/2-1/3 больше объема разводимого вещества. [c.410]
Двухкомпонентные растворы реальных веществ, отклоняющиеся в своем поведении от идеального и относящиеся к первому виду растворов, т. е. к растворам компонентов, смешивающихся во всех отношениях, различаются между собой по характеру их отклонения, положительному или отрицательному, от идеального линейного закона, выражающего суммарную упругость пара раствора в функции мольного состава жидкой фазы. [c.11]
Таким образом, для рассматриваемого вида кривой растворимости компонентов системы, двухколонная с отстойником ректификационная установка приходит к ранее рассмотренной схеме одной полной и одной лютерной колонны, применяемой при фракционировке однородных в жидкой фазе растворов частично растворимых веществ. [c.117]
Жидкая фаза, экстрагирующая целевое вещество из исходного раствора, называется экстрагентом. Раствор целевого вещества в экстрагенте называется экстрактом. Исходная жидкая фаза, освобожденная в результате экстракции от целевого вещества, называется рафинатом. [c.97]
Свойства как газов, так и жидкостей и твердых тел при давлениях, отличающихся от атмосферного, определяются по величинам, найденным для стандартного состояния, с использованием основных термодинамических соотношений, в которые входит сжимаемость вещества. В ряде случаев полезными оказываются данные о давлении пара. Читателю, желающему найти подробное описание методов исследования и интересующемуся закономерностями для растворов твердых и жидких веществ, следует обратиться к общим учебникам по термодинамике. [c.365]
В задачу этой главы не входит описание состояния равновесия твердых и жидких веществ. Читателя, интересующегося этим вопросом, следует отослать к обычным учебникам [6, 7]. Тем ие менее в случаях, когда в газообразной фазе находятся компоненты жидкого раствора, расчет равновесия для жидкости не представляет трудности. [c.368]
Измельчение твердых веществ и смешивание как твердых, так и жидких веществ в практике химических лабораторий проводится часто. Все твердые материалы, поступающие в лабораторию для анализа, обязательно измельчают. Перед приготовлением растворов твердых веществ 1и также полезно предварительно измельчить. Для получения однородной смеси различных твердых веществ необходимо, чтобы смешиваемые твердые вещества были измельчены как можно тщательнее. [c.97]
Обычно теплота растворения рассчитывается на моль растворенного вещества, однако для растворов жидких компонентов она нередко относится к одному молю раствора. [c.70]
На этом рисунке кривая AD показывает зависимость давления насыщенного пара чистого жидкого растворителя от температуры, кривая БС—давление пара чистого твердого растворителя, кривые Л D, А» D» и давление пара растворителя над растворами нелетучего вещества с постоянными концентрациями х [c.233]
Рассмотренные выше закономерности, относящиеся к растворимости твердых веществ в жидкости и понижению точки затвердевания растворов, имеют место в том случае, когда из раствора выделяются чистые твердые компоненты. Между тем нередко при охлаждении раствора выделяются твердые растворы—однородные кристаллические фазы переменного состава, состоящие из двух или нескольких компонентов. В этом случае давление пара компонента над твердым раствором (кривая Ьс на рис. VII, 5) меньше, чем над чистой твердой фазой (кривая ВС), и равновесие жидкого и твердого раствора осуществляется не при температуре Т , которой отвечает точка С, а при более высокой температуре Т , определяемой точкой с пересечения кривой D (давление пара над жидким раствором) с кривой Ьс. При этом температура может быть ниже Го—температуры затвердевания чистого растворителя (рис. VII, 5а) или выше ее (рис. VII, 56). [c.237]
Жидкие трехкомпонентные системы могут состоять из жидких веществ, как дающих растворы любого состава, так и взаимно ограниченно растворимых. В последнем случае на диаграмме состояния появляется область расслаивания. Фигуративной точке системы, лежащей внутри этой области, отвечают фазовые фигуративные точки двух растворов, на которые распадается система. Так же как и в двух компонентных системах, взаимная растворимость трех компонентов зависит от температуры, и в некоторых случаях при соответствующей критической температуре наступает взаимная неограниченная растворимость всех трех компонентов. Область ограниченной растворимости может иметь различные очертания. [c.433]
Значительное различие в энергиях взаимодействия между молекулами компонентов двухкомпонентной жидкой системы приводит к нарушению гомогенности системы. Обе жидкости А и В оказываются растворимыми только до определенного предела. При прибавлении жидкости В к А при некоторой ее концентрации нао.в образуется раствор жидкого вещества А, насыщенного В. [c.170]
Рассмотрены закономерности растворимости, различные фазы и фазовые равновесия растворов низкомолекулярных веществ, растворов полимфов и лиотропных жидких кристаллов, особе1 ности набухания лиотропных жидких кристаллов и полимеров. [c.2]
Для водных растворов, жидких веществ часто приводят их объемную концентрацию так, например, в 1 л 20 %-ного раствора глицерина содернштся 20 см глицерина. [c.20]
Принципиальный интерес представляло количественное изучение капсулирования двухкомпонентных растворов жидких веществ с близкими физическими свойствами, но с различной физической активностью по отношению к деформируемой полимерной пленке. Одна жидкость должна поглощаться полимером и образовывать структурные капсулы при изометрической термообработке пленки. Вторая должна быть физически и химически инертной по отношению к полимеру, но неограниченно смешиваться с первой жидкостью в интервале температур вытяжки и термообработки. Кроме того, жидкости должны быть надежно разделимы хроматографически. Использование метода газовой хроматографии для оценки концентрации капсулируемых растворов и совместимость компонентов определили конкретный состав модельных растворов. [c.89]
Вышеизложенное поясняет значение полярности молекул растворителя чем больше их дипольный момент (и, следовательно, выше диэлектрическая постоянная), тем выше их способность сольватировать, тем больше выделяется энергии и лучше идет растворение. С другой стороны, способность твердых и жидких веществ растворяться также в значительной мере зависит от полярности их собственных молекул. Хорошая растворимость, например, сахаров, не обра- [c.24]
В жидких растворах частицы растворенного вещества связаны с окружающими их частицами растворителя. Эти комплексы называются сольватами, а для водных растворов гидратами. Подобное представление о растворах возникло еще в 60-х годах XIX в. в результате работ Д. И. Менделеева. На основании экспериментальных фактов он выдвинул предположение о существовании в растворах определенных химических соединений растворенного вещества с водог. Эта идея составила основу химической теории растворов. Химическая теория растворов принципиально отличается от фи-зическсй теории, которая рассматривала растворитель как инертную среду и приравнивал,а растворы к простым механическим смесям [c.127]
Когда один из слоев жидкой фазы полностью выкипает, то система из трехфазнон и соответственно, одновариантной, становится двухфазной и двухвариантной, т. е. приобретает еще одну дополнительную степень свободы. Поэтому в случаях парожидкого равновесия одной жидкой и одной паровой фазы в системе частично растворимых веществ при заданном внешнем давлении температура системы не сохраняет постоянного значения в ходе перегонки и, по мере ее протекания, прогрессивно растет. Изобарные равновесные кривые точек кипения гомогенных в жидкой фазе растворов Z., и даются соответственно ветвями СА и BD общей кривой кипения ABD, горизонтальный участок АВ которой относится исключительно к неоднородным жидким растворам. Изобарные равновесные кривые точек конденсации паров, отвечающих условию равновесия с однофазными жидкими растворами и 2 даются соответственно ветвями СЕ и DE. [c.26]
Как известно, конвертированный и коксовый газ содержит взрывоопасные и токсичные вещества. Растворы моноэтаноламина и метанола, применяемые для очистки газов, токсичны, а жидкий азот при попадании на колпроцессы очистки идут при высоких и очень низких температурах. Возможность возникновения пожара или взрыва, отравления или получения ожога может создаваться при нарушениях технологического режима, подсосе воздуха в газ или в результате образования в производственных помещениях взрывоопасных и отравляющих газовоздушных смесей при прорыве газов и жидкостей через неплотности оборудования, коммуникаций и запорной арматуры. Поэтому герметичность оборудования и трубопроводов отделения очистки должны проверяться ежесменно. Запрещается подтягивать крепежные детали фланцевых соединений для ликвидации пропусков газов и жидкостей, если система находится под избыточным давлением. Давление следует повышать и снижать постепенно, по установленному для данного оборудования регламенту. Инертный газ, применяемый для продувок, должен содержать не более 3% (об.) кислорода и совершенно не иметь горючих примесей. Перед продувкой газ должен подвергаться анализу. [c.52]
Образующаяся при экстракции тяжелая фаза (раствор асфальтовых веществ в пропане) опускается, а легкая фаза (рафииатный раствор, состоящий в основном из жидкого пропана и масляной части) поднимается. [c.153]
chem21.info
Жидкий раствор — Большая Энциклопедия Нефти и Газа, статья, страница 1
Жидкий раствор
Cтраница 1
Жидкие растворы занимают промежуточное положение между химическими соединениями постоянного состава и механическими смесями. Как и химические соединения, они однородны и характеризуются тепловыми явлениями, а также контракцией — часто наблюдающимся сокращением объема при смешивании жидкостей. С другой стороны, в отличие от химических соединений растворы не подчиняются закону постоянства состава; они, как и смеси, могут быть легко разделены на составные части. [1]
Жидкие растворы могут быть построены по типу жидкость — газ; жидкость — жидкость; жидкость — твердое тело. Это наиболее часто встречающиеся и наиболее изученные системы. Они имеют большое значение в биологических процессах и химической, машиностроительной и приборостроительной технологии. [2]
Жидкий раствор с температурой, близкой к температуре кипения, подается к нижнему концу трубки. Чуть выше конца трубки начинается кипение, благодаря чему объем парообразной фазы многократно увеличивается. Образующийся пар идет к свободному верхнему концу трубки, при этом в результате трения жидкость поднимается тонким слоем по внутренней стенке трубки. По мере испарения жидкости дополнительно возникает пар. С увеличением скорости пара увеличивается касательное напряжение, возникающее в результате трения молекул на г. рани раздела фаз и увеличивается скорость движения жидкости, которая в верхнем конце трубки часто достигает 20 м / сек. [3]
Жидкий раствор, находящийся в состоянии термодинамического равновесия, не является, естественно, статической конструкцией. Можно говорить о среднем времени жизни сольватных комплексов и пребывания частиц в нем. Здесь мы не рассматриваем эту сторону явления, успешно разрабатываемую школой О. Я. Самойлова [ 6 ( см. также стр. [4]
Жидкие растворы по своей природе, свойствам, характеру взаимодействий между частицами очень разнообразны, в связи с чем трудно создать единую количественную теорию, описывающую поведение различных растворов в широкой области концентраций. Наука о растворах — одна из наиболее старых областей естествознания, в развитие которой сделан вклад многими исследователями. В ходе развития учения о растворах были высказаны две точки зрения на природу растворов — физическая и химическая. Количественные законы ( законы Вант-Гоффа, Рауля) были открыты в предположении, что в разбавленных растворах молекулы растворенного вещества подобны молекулам идеального газа. Отступления от этих законов, наблюдаемые для растворов электролитов, были объяснены на основе теории электролитической диссоциации Аррениуса. [5]
Жидкий раствор, находящийся в состоянии термодинамического равновесия, не является, естественно, статической конструкцией. Можно говорить о среднем времени жизни сольватных комплексов и пребывания частиц в нем. [6]
Жидкие растворы в свою очередь подразделяются на растворы газов в жидкостях; растворы твердых веществ в жидкостях; растворы жидкостей в жидкостях. [8]
Жидкий раствор должен быть идеальным или достаточно разбавленным, чтобы подчиняться закону Рауля. [9]
Жидкий раствор должен быть идеальным или достаточно разбавленным, чтобы подчиняться закону Рауля. [10]
Жидкие растворы, как и индивидуальные жидкости, обладают внутренней структурой ближнего порядка. При этом структура разбавленных растворов близка к структуре растворителя, а концентрированных — к структуре растворенного вещества. [11]
Жидкий раствор, образующийся на базе железа, представляет собой конденсированную фазу, не обладающую дальним порядком в размещении атомов. [12]
Жидкие растворы — большая и важная группа растворов, в свою очередь, подразделяется на: 1) растворы твердых тел в жидкостях, 2) растворы жидкостей в жидкостях, 3) растворы газов в жидкостях. [13]
Жидкие растворы идеальные 175, 179 ел. [14]
Страницы: 1 2 3 4
www.ngpedia.ru
Раствор жидкостей — Справочник химика 21
Растворы жидкостей в жидкостях очень разнообразны по своей природе и свойствам. Растворимость жидкостей в жидкостях зависит от природы растворителя и растворяемого вещества, температуры, присутствия в растворе посторонних веществ. Существуют раство- [c.385]Спектры растворов, жидкостей и кристаллов могут служить важным источником сведений о межмолекулярном взаимодействии, о его тонких деталях. Сравнивая величину низкочастотного сдвига при растворении вещества в серии растворителей, можно определить, как изменяется энергия межмолекулярного взаимодействия веществ с растворителем, электронно-донорные свойства растворителей и др. Особое значение при изучении межмолекулярного взаимодействия приобрела спектроскопия водородной связи. [c.178]
Первые работы Дж. Гильдебранда связаны с обоснованием закономерностей идеальных растворов. Им показано, что если при образовании раствора теплота растворения кристаллов соответствует скрытой теплоте плавления и растворы образуются без изменения суммы объемов, растворы следуют закону Рауля [61]. Рассматривая механизм внутримолекулярного взаимодействия в растворе, Дж. Гильдебранд ввел понятие о внутреннем давлении. Жидкости с равными внутренними давлениями образуют идеальный раствор. Жидкости с близкими внутренними давлениями и близкой полярностью взаимно растворимы в широком диапазоне концентраций. Для оценки энергии связи сил межмолекулярного взаимодействия им использованы величины скрытой теплоты испарения. Растворы с дисперсионными силами взаимодействия, у которых теплоты, смешения имеют низкие значения, а изменение энтропии происходит по закону идеальных газов, были выделены в отдельный класс, полу- [c.213]
Аккомодационные соотношения (1.46), (1.47) требуют определения парциальных удельных энтальпий компонентов в фазах при равновесии. Для смеси газов (паров) при невысоких давлениях, а также для жидких растворов, теплота смещения компонентов в которых мала, парциальные характеристики смеси близки к соответствующим характеристикам чистых компонентов. Однако в неидеальных смесях (т. е. значительно отклоняющихся от закона Дальтона — для газов или от закона Рауля — для растворов жидкостей) парциальные характеристики зависят от состава смеси и представляются в виде [39] [c.52]
Весьма важной является часть 4 книги, посвященная рассмотрению кинетики и механизмов реакций в конденсированной фазе (в растворах, жидкостях), реакций с участием твердых поверхностей, процессов, связанных с образованием новой фазы, и ферментативных реакций. [c.6]
Растворы различают газообразные, жидкие и твердые. Газообразные растворы обычно представляют собой смеси газов и реже растворы жидкостей или твердых веществ в газах. Под жидкими растворами понимают растворы, полученные смешением жидкостей, растворением твердых веществ или газов в жидкостях и плавлением твердых систем, содержащих более одного компонента. Твердые растворы — это твердые фазы переменного состава. Они могут быть получены при охлаждении жидких расплавов или при растворении газов в твердых веществах. [c.338]
РАСТВОРЫ ЖИДКОСТЕЙ В ЖИДКОСТЯХ [c.196]
Рафинат, недонасыщенный растворите- Жидкость при температуре ниже темпе- [c.92]
Таким образом, диффузионные следы частиц, расположенных выше по потоку, обедняют раствор жидкости, приходящей в диффузионный пограничный слой следующей частицы. [c.131]
Водные растворы жидкостей, разбавленная кислота, жиры и минеральные масла [c.300]
ПЕРЕГОНКА РАСТВОРОВ ЖИДКОСТЕЙ, ОБРАЗУЮЩИХ ГОМОГЕННЫЕ АЗЕОТРОПЫ [c.287]
Заменяют в реакторе воду взвешенным исследуемым раствором (жидкостью) (500 см ). Повторив измерение находят [c.55]
Жидкие растворы в свою очередь подразделяются на растворы газов в жидкостях, растворы жидкостей в жидкостях, растворы твердых тел в жидкостях. [c.80]
Схема эксперимента МКД аналогична КД (см. гл. IX). После четвертьволновой пластинки лучи с круговой поляризацией г и I проходят через кювету, находящуюся в поле В. Обычно исследуют растворы, жидкости или твердые тела. [c.257]
Плотность раствора (жидкости) вычисляют по формуле [c.93]
Константа равновесия К в данном случае называется коэффициентом распределения, а соотношение (2.53) представляет собой закон распределения . Соотношение (2.53) можно рассматривать как пример применения уравнения (2.28). На законе распределения основана широко Применяемая в промышленности экстракция — процесс извлечения вещества из раствора в слой другой, ие смешивающейся с раствором жидкости (экстрагента). [c.251]
Для измерения плотности раствора жидкость наливают в цилиндр и осторожно опускают в нее ареометр. Измерение производят, если ареометр свободно плавает в растворе, не касаясь дна и стенок цилиндра. Плотность раствора определяется делением шкалы ареометра, до которого он погружается в раствор. Отсчет производят по нижнему краю мениска. По величине зкснерименталь- [c.48]
Глава IX. Растворы жидкостей в жидкостях………… [c.492]
Закон Рауля следует из зависимости (V. 53) и условий равновесия = между раствором (жидкостью) и паром предполагается при этом, что пар ведет себя как идеальный газ. Действительно [c.240]
Нельзя выпаривать на рабочих столах вещества, образующие, вредные газы, например кислоты, аммиачные растворы, жидкости, содержащие сероводород, хлор, бром, хлористоводородную кислоту и т. д. [c.8]
Для равновесия раствор (жидкость)—газ (пар) так же, как для кристаллической фазы, запишем [c.98]
Расположение точки А на диаграмме равновесия между составом Л в второго жидкого слоя В и составом Уе пара Е, равновесного двухслойной жидкости, показывает, что для неэвтектического типа растворов жидкость состава л л, представленная фигуративной точкой А, должна в процессе испарения постепенно поглощаться, выделяя из своей массы пар состава уе и жидкую фазу состава хв. Имея в виду постоянство в ходе перегонки составов Ха и л в обоих жидких слоев, невозможно иначе представить процесс выделения из жидких фаз пара, более богатого компонентом а, чем оба перегоняющихся слоя. [c.53]
Сколько вещества растворяется в определенном количестве воды Представьте, что вы готовите раствор нитрата калия (КЫО,). Вы наливаете воду в стакан и добавляете полную ложку твердых, белых кристаллов нитрата калия. После того как вы перемешаете воду, твердые кристаллы растворятся. Жидкость останется бесцветной и прозрачной. В полученном растворе вода — растворитель, а нитрат калия — растворенное веществи. [c.52]
Коистаггта равновесия К в данном случае называется коэффициентом распределения, а (2.53) — законом распределения . Соотношение (2.53) можно рассматривать как пример применения уравнепия (2.28). На законе распределения основан широко применяемый в промышленности процесс экстракции — извлечения вещества нз раствора в слой другой, несмен1ивающейся с раствором жидкости — экстрагента. [c.234]
Все реальные растворы жидкостей, неограниченно растворимых друг в друге в той или иной степени, дают отклонения от закона Рауля. Эти отклонения могут быть либо положительными, когда парциальные давления компонейтов, а следовательно, и общее давление паров больше, чем для идеальных растворов, либо отрицательными, когда рд, рв и р меньше, чем следует из закона Рауля, [c.258]
В химической технологии ширеко распространены и имеют важное значение процессы массопередачи, характеризуемые пере-хоцом одного или нескольких веществ из одной фазы в другую. Путем переноса вдного или более компонентов из фазы в фазу можно разделять как гетерогенные, так и гомогенные системы (газовые смеси, растворы жидкостей и др.), причем наиболее часто процессы массопередачи используют для разделения ромогенных систем. [c.382]
Растворение различных веществ в воде сопровождается выделением или поглощением тепла. В общем случае растворение есть сложный физико-химический процесс, тепловой эффект которого Р раств. алгебраически складывается из теплоты сольватации Рс (экзотермический процесс), теплоты, затрачиваемой на разрушение кристаллической решетки Рразр. или на испарение (если растворяется жидкость в жидкости), и теплоты, затрачиваемой на распределение сольватированных частиц по всему раствору Рдифф. Так как энергия Рдифф. обычно мала, то ею можно пренебречь. Тогда [c.35]
ГЛИНИСТЫЕ РАСТВОРЫ — жидкости, применяемые для промывки при бурении скважин. Г. р.— многокомпонентные системы состоят из воды, глины, улек-тролнтов, органических веществ и инертных наполнителей. Проходка глубоких скважин практически невозможне, без применения Г. р. [c.77]
Для приготовления второго раствора взять 5,8 г KS N или 4,6 г Nh5S N и 200 мл воды. Далее налить в большую колбу около 1 л воды и 8—12 мл каждого из приготовленных растворов. Жидкость окрашивается в красновато-оранжевый цвет. Окраска не должна быть темной. [c.45]
Постоянная С может бьать определена из следующих соображений. При температуре плавления твердое тело приобретает свойства жидкости, и, следовательно, возможна любая растворимость, так как при образовании идеального раствора жидкости смешиваются во всех отношениях. В пределе мольная доля растворенного вещества = . [c.217]
chem21.info
Растворы жидкие — Справочник химика 21
Раствор жидкого стекла [c.35]
Процесс приготовления гелеобразующего раствора жидкого стекла из силикат-глыбы включает стадии дробления силикат-глыбы, ее растворения, фильтрования полученного раствора и разбавления его водой до требуемой концентрации (рис. 2). [c.35]
При смешении водных растворов жидкого стекла и серной кислоты выпадение в осадок нерастворимого соединения (геля) происходит всегда, вне зависимости от соотношения взятых растворов. Количество осадка определяется минимальной концентрацией серной кислоты — порогом коагуляции. Скорость коагуляции золя кремневой кислоты зависит от температуры смеси гелеобразующих растворов, концентрации ЗЮг в растворе, pH среды, применяемой кислоты (серная или соляная). Скорость коагуляции растет при повышении температуры и концентрации исходного коллоидного раствора и при понижении вязкости особенно сильно на вязкость раствора влияет температура. [c.47]
Контактирование сырья с кислотой осуществляют обычно в цилиндрических мешалках с коническим дном. Продолжительность перемешивания 30 — 80 мин (зависит от интенсивности работы мешалки и требуемой глубины очистки), время отстаивания кислого гудрона до 10 ч. Для ускорения осаждения используют часто коагулянты (раствор жидкого стекла или едкого натра) или применяют электроразделители. [c.277]
Растворы жидких металлов и нх солей [c.297]
К процессам депарафинизации кристаллизацией из углеводородных растворителей-разбавителей относятся две группы процессов, существенно отличающихся друг от друга по технологическому оформлению группа процессов депарафинизации в растворе жидких углеводородов, в частности бензиновых фракций, и группа процессов депарафинизации в растворе сжиженных углеводородных газов — пропана, бутана, главным образом в растворе пропана. [c.173]
Сухой природный каучук в растворе жидкого хлора хлорируется при —70° только до образования соединения, содержащего 54% хлора. Каучук набухает в жидком хлоре прп —70° и в течение 17 час. хлорируется до производных, содержащих 38—43% хлора, но нагретый до 120° этот продукт уже через 1—3 часа содержит 68—69% хлора. При нагревании в течение 2 час. при 90° под давлением 13 ат получается продукт с 68,5% хлора [35]. [c.220]
Степень ионизации активных групп зависит главным образом от их химической природы и от свойств внешнего раствора (жидкой фазы). Так, например, катиониты, содержащие активные сульфогруппы, хорошо ионизуются и поэтому осуществляют обмен в широком интервале pH. Такая группа, как карбоксильная, в нейтральных или кислых средах большей частью находится в недиссоциированном состоянии в виде —СООН. В зависимости от константы диссоциации катионита в водородной форме (Н-форме) различают сильнокислотные и слабокислотные иониты. Как будет показано далее, синтез дифенилолпропана катализируется сильнокислотными ионитами. К ним относятся катиониты КУ-1, СБС и КУ-2, выпускаемые в СССР в промышленном масштабе. [c.143]
Ниже приведена молекулярная масса полиизобутилена, полученного полимеризацией изобутилена трифторидом бора в растворе жидкого этилена в присутствии диизобутилена. [c.334]
Обычно теплота растворения рассчитывается на моль растворенного вещества, однако для растворов жидких компонентов она нередко относится к одному молю раствора. [c.70]
В производстве микросферических природных и синтетических катализаторов и адсорбентов суспензию получают при осаждении гелеобразующего раствора жидкого стекла раствором сернокислого алюминия (или сернокислого магния). Эмульсией является водный раствор нейтрализованных контактов. Приготовлением суспензии занимается формовочно-промывочное отделение, эмульсии — узел регенерации. [c.35]
Если оба раствора, жидкий и твердый, разбавлены, то [c.238]
Можно также изготовить концентрационные элементы, в которых электродами являются растворы (жидкие или твердые) одного и того же металла в другом, более положительном (на- [c.564]
Формование — один из основных технологических процессов в производстве катализаторов и адсорбентов в результате этой стадии закладываются форма, структура и качество будущего продукта. Первичное взаимодействие растворов жидкого стекла и сернокислого алюминия (или магния) при синтезе катализатора протекает в коллоидном растворе (золе) с образованием частиц различной формы и размера — микросфер, крупных шариков, таблеток и др. Схема первичного синтеза алюмосиликатного катализатора примерно выражается следующим уравнением [c.45]
Газы тем более растворены в нефти, чем больше давление, под которым нефть находится в недрах земли. Явление фонтанов по суш,еству есть естественное выделение газов благодаря искусственному понижению давления в пласте, когда высвобождаю-ш иеся газы увлекают с собой и самую нефть. Но в уже добытой нефти остаюш,неся в ней растворенные газы легко выделяются с повышением температуры нефти. В противоположность им жидкие метановые углеводороды (парафины) с высокой температурой кристаллизации извлекаются из нефти или из содержаш,их парафин дестиллатов лишь при понижении температуры, при которой наступает кристаллизация парафинов из раствора жидких углеводородов. [c.78]
Гелеобразующими растворами в производстве катализаторов и адсорбентов являются коллоидные растворы жидкого стекла, сернокислого алюминия и сернокислого магния. Приготовлением всех этих растворов занимаются сырьевые установки (или блоки), на которых сосредоточены все запасы сырья и реагентов. [c.35]
Фильтрование раствора жидкого стекла, загрязненного механическими примесями, осуществляют на фильтр-прессе-8, а оттуда чистый раствор направляют в емкость 9 для приготовления рабочего раствора (рис. 2). Для фильтрования применяют рамный фильтр-пресс с салфетками из специальной ткани — бельтинга. Скорость фильтрования зависит от модуля силикат-глыбы, температуры и плотности раствора, качества фильтрующих салфеток. [c.37]
Разбавление раствора жидкого стекла проводят из отфильтрованного раствора до концентрации 1,1 —1,2 н. Раствор жидкого стекла в емкости тщательно перемешивают воздухом в течение 30—40 мин и отбирают пробу. По данным анализа подсчитывают количество воды, необходимое для приготовления рабочего раствора. Особое внимание нужно уделять тщательности перемешивания раствора. [c.38]
Приготовленный раствор жидкого стекла является одним из гелеобразующих рабочих растворов и поступает на процесс формования катализатора. Перед формованием его еще раз перемешивают воздухом и повторно определяют концентрацию (контрольный анализ). Без контрольного анализа раствор брать не рекомендуется так как при хранении его в емкости (а тем более при длительном хранении) в раствор может попасть вода или растворы другой концентрации, т. е. нормальность рабочего раствора изменится. Качество раствора жидкого стекла устанавливают по плотности и количеству окиси натрия, определенного титрованием. Эти две величины позволяют ориентировочно найти модуль силикат-глыбы. Для точ- [c.38]
При формовании силикагелей раствор жидкого стекла осаждают водным раствором серной кислоты. При этом образуется золь крем- [c.46]
Исправление подкисленной формовочной воды при незначительном понижении величины ее pH допускается щелочью (едким натром). При значительном подкислении проводят полную замену формовочной воды в системе узла формования. Подщелачивание подкисленной формовочной воды раствором жидкого стекла не допускается. [c.50]
Замерзание раствора жидкого стекла в холодильнике ликвидируют следующим образом. Закрывают возврат рассола из холодильника в аммиачную компрессорную и открывают задвижку в канализацию. В рассольную (меж-трубную) часть холодильника подают горячую воду и прокачивают ее до тех пор, пока через ротаметр не пойдет раствор жидкого стекла. Прекращают подачу горячей воды, открывают задвижку на линии возврата рассола на холодильную установку и возобновляют процесс формования катализатора. [c.50]
Перед началом формования из сырьевой установки принимают исходные растворы жидкого стекла и сернокислого алюминия, проверяют их концентрацию и осветление раствор сернокислого алюминия подкисляют серной кислотой. Осветление растворов имеет немаловажное значение мутные растворы указывают на присутствие в них посторонних механических примесей, отрицательно влияющих на качество катализатора. Подкисление способствует [c.51]
Сырьевое отделение состоит из двух блоков. Силикат-глыба дробится на щековой дробилке 1 на мелкие куски и с помощью электротельфера 2 и бадьи загружается в вертикальный реактор-автоклав 3. Полученный в автоклаве концентрированный раствор жидкого стекла выдавливают в аппарат 4, там разбавляют паровым конденсатом (или смесью конденсата с умягченной водой) и насосом откачивают в емкость 5 для приготовления гелеобразующего раствора путем разбавления его водой. Перед этим раствор обязательно фильтруют (на схеме не показано). [c.79]
В промывочный чан 26, промежуточную емкость 25 и формовочную колонну 23 насосом пз резервуара 24 закачивают паровой конденсат, а из мерника 20 насосом в колонну 23 направляют формовочное масло и налаживают циркуляцию формовочной воды (конденсата) по схеме насос — формовочная колонна 23 — промывочный чан 26 — промежуточная емкость 25. Исходные рабочие растворы жидкого стекла и сернокислого алюминия из соответствующих емкостей 5 п 10 насосами закачивают в напорные бачки 6, из которых под определенным давлением через холодильники 7 и ротаметры 8 подают в смеситель-распылитель 9. Образовавшийся в смесителе гидрозоль воздухом распыляется в формовочное масло. В холодильниках 7 рабочие растворы охлаждаются рассолом, поступающим нз аммиачно-холодильной установки. [c.79]
Включают в ра боту вертикальный элеватор 16, ковши которого поднимают гидроокись алюминия наверх, где она взвешивается и, во избежание выброса раствора кислоты, медленно ссыпается в реактор 15. Разваривают гидроокись алюминия путем ввода в реактор острого водяного пара. Полученный раствор сернокислого алюминия подкисляют серной кислотой в емкости 17. Растворы жидкого стекла и сернокислого алюминия фильтруют на фильтр-прессах 10 и 13 и разбавляют водой до концентрации рабочих растворов в аппаратах 11 и 18. [c.83]
Таким образом, из-за проскоков взвешенных частиц в рабочий раствор, самокоагуляции раствора жидкого стекла и невозможности быстро освободиться от этих примесей обычными фильтрующими материалами (мешковина, бельтинг) получающиеся шарики гидрогеля сильно растрескиваются при сушке. Например, при работе в нормальных условиях на содовой силикат-глыбе растрескивание шариков гидрогеля обычно не превышает 12—14%, при работе с мутным сульфатным жидким стеклом в зависимости от степени его коллоидности и концентрации взвешенных частиц выход растрескивающихся шариков после сушки гидрогеля достигает 30—40%. [c.28]
Технологическая схема формовочно-промывочного отделения заключается в следующем. Первый поток — раствор жидкого стекла — из емкости подают насосом в холодильник предварительного охлаждения и далее в напорный бачок. Из напорного бачка, пройдя рассольный холодильник, раствор через ротаметры поступает к боковым ниппелям смесителей инжекторного типа под давлением 3—3,2 ат. [c.84]
На узле формования несколько изменен технологический режим. Концентрация раствора жидкого стекла принята 1,41 —1,43 н. вместо 1,18—1,20 н., а подкисление раствора сернокислого алюминия принято 68—71 г/л вместо 53—56 г/л. Повышено давление в напорно-буферной системе 3,2 ат (вместо 3,0 ат) для жидкого стекла, [c.90]
Мак Колей и Лии [212] заметили, что растворимость ксилолов и болео метилированных бензолов в жидком фтористом водороде необычайно сильно возрастает при добавлении к системе трехфторнстого бора. В самом деле, на каждый моль поглощенного трехфторнстого бора в растворе жидкого фтористого водорода переходит в раствор 1 моль ароматического углеводорода. [c.402]
С экономической точки зрения очень важно оптимально использовать агент сульфирования — Н.2504. В самом деле, вследствие нестабильности продуктов в присутствии Н2304 невозможно сдвинуть, равновесие сульфирования в сторону образования сульфокислот посредством непрерывного удаления образующейся воды (например, азеотропной перегонкой). Поэтому сульфирование проводят олеумом (20% 50з) при температуре около 25—30 °С, газообразным 50з, разбавленным инертными газами, или в растворе жидкой ЗОз. При этом достигают практически полного, а следовательно, экономичного-использования агента сульфирования кроме того, вторичных продуктов образуется немного. [c.341]
О соинициирующей активности ряда гидроксилсодержащих соединений при полимеризации изобутилена в растворе жидкого этилена в присутствии трифторида бора можно судить по данным, приведенным на рис. 1—3 [20]. [c.333]
Товарное жидкое стекло разбавляется водой до получения раствора с плотностью 1,4. Этот раствор смешивается с равным объемом воды и титрованием пробы смеси устанавливается количество НС1, необходимое для полной нейтрализации. Затем к разбавленному водой жидкому стеклу приливается при перемешивании 5 и. раствор H I, взятый с 20 %-нь)М избытком. Образовавшийся гель, который после застывания разламывается на куски, отмывается горячей водой до удаления следов иона хлора и переносится в 0,2 п. раствор сульфата алюминия, причем количество последнего берется из расчета 200 мл на 100 мл раствора жидкого стекла. (]1месь геля исул1,фата алюминия нагревается 3—4 ч па водяной бане, а затем, овгорячей водой до исчезновения иона SO4. Для полного удаления сульфатов гель повторно кипятят с водой, затем отделяют от воды и просушивают в сушильном шкафу. В процессе сушки температура в течение 6 ч медленно новыша( тся от комнатной до 110 °С. Высушенный таким образом гель активируется пропусканием через него воздуха при 350 °С в продолжение 2—3 ч. [c.56]
После испытания нескольких конструкций мы остановились на смесителе-распылителе типа форсунки (рис. 1). Раствор сульфата а гюминия подается через верхний боковой цатрубок 1 и через сопло 2 попадает в смеситель 3. Раствор жидкого стекла поступает через — средний боковой патрубок 4 ш по коль- [c.210]
При формовании катализатора требуется постоянная, относп-тельно низкая температура гелеобразующих растворов. Повышенпе температуры ускоряет процесс коагуляции и усложняет формование. Охлаждают растворы в холодильниках 7. Схема холодильной установки и циркуляции рассола приведена на рис. 6. Аммиачнохолодильная установка состоит пз аммиачного компрессора 1, испарителя 2, конденсатора 4 и вспомогательной аппаратуры. Охлажденный до 5—6° С рассол из рассольной ванны 3 насосом подают в холодильник 5, в котором охлаждают рабочие растворы жидкого стекла [c.48]
Приготовление исходных растворов. Раствор жидкого стекла получают из т KJrouиднoгo силиката натрия (силикат-глыбы), куски которого дробятся на щековой дробилке. В реактор I (рис. 4) с помоп1,ью тельфера загружается необходимое количество дробленого силиката натрия, где с помощью водяного пара производится его разварка. Раствор кидкого стекла (4,0— [c.222]
Формовка микрошарикового катализатора. Раствор жидкого стекла перекачивается в рг шорный бачок 8, откуда под давлением 0,3 МПа через змеевиковый холодильник 9 поступает в смеситель 10. Туда же из напорного бачка 8 под давлением 0,15 МПа через змеевик 9 подается раствор сульфата алюминия. В смесителе 10 образуется золь алюмосиликата, которьсй с помощью сжатого воздуза разбрызгивается в формовочную колонну 11, заполненную формовочным маслом (смесь трансформаторного масла с керосином).. [c.223]
Вертикальный автоклав заливают на /з объема паровым конденсатом или умягченной водой и затем загружают силикат-глыбу. Люк герметически закрывают и в автоклав вводят острый пар. Во избежание гидравлических ударов осторожно открывают паровую задвижку, увеличивая подачу пара по мере прогрева воды внутри автоклава. При давлении 4—4,5 ат подачу пара прекращают (после закрытия паровой задвижки давление поднимается с 4 до 5 ат за счет процесса растворения силикат-глыбы, в дальнейшем давление постепенно падает). Растворение глыбы продолжается 4—5 ч в течение этого времени давление в автоклаве поддерживают в пределах 4,8—5,0 ат периодической подачей пара. Иногда давление в автоклаве может подняться выше давления в линип острого пара. В результате раствор жидкого стекла может попасть в паропровод и далее, через паровые насосы, в линию мятого пара, а через конденсатную станцию — в конденсатные резервуары. Для предотвращения этого вертикальный автоклав оснащен предохранительным клапаном, отрегулированным на рабочее давление, а на линии острого пара имеется дренажная линия между двумя задвижками, которая при работе автоклава всегда открыта. [c.36]
Получив результаты лабораторных анализов, заполняют всю спстед1у узла формования рабочими растворами жидкого стекла и подкисленного сернокислого алюминия и налаживают их циркуляцию через напорно-буферную систему. Из емкостей 1 п 2 рабочие растворы самостоятельными потоками через холодильники 8 предварительного охлаждения насосами подают в соответствующие напорные бачки 5, из которых они поступают в буферные емкости 6. Буферные емкости снабжены регуляторами уровней, с подющью которых избытки рабочих растворов возвращают в рабочие емкости [c.52]
После проведения циркуляции в напорных бачках создают статическое давление посредством сжатого воздуха. Одновременно проводят сборку смесителей, проверяют правильность установки формующих конусов, регулируют их параллельность и расстояние до поверхности масла, проверяют центровку (соосность) смесителей и конусов и регулируют расстояние между нижними концами успокоительных труб ок смесителей и вершинами конусов. Затем смесители отводят от формовочных колонн к сливным воронкам и открывают вентили перед ротаметрами, установленными на заданный расход рабочих растворов в соотношении примерно 2 1 (раствор жидкого стекла 550—650 л мин, сернокислого алюминия 200— 2Ъ0 л/мин). Колебание в соотношении рабочих растворов не должно превышать 0,3—0,5, ). В процессе производства шарикового катализатора необходима точная дозировка гелеобразующих растворов, так как от этого зависит не только качество продукта, но и воздюжность образования шариков нужной форд1Ы и размера. Достигается это придхепепием электронных ротаметров п механических клапанов, установленных на каждод потоке рабочих растворов. [c.52]
Вторым непременным условием является быстрое и тщательное смешение гелеобразующих рабочих растворов в смесителе. Рабочие растворы жидкого стекла и сернокислого алюмпния поступают в смеситель под давлениед соответственно 3 и 1,8 ат. В результате создается турбулентное движение, обеспечивающее хорошее смешение растворов. Из камеры смешения смесь рабочих растворов (золь) поступает в успокоитель, где турбулентная струя переходит в ламп- [c.52]
Быстрое развитие каталитического крекинга связано с широким применением синтетического алюмосиликатного шарикового катализатора. Шариковый катализатор (85—87% ЗЮг и 13—15% А12О3) сформован методом совместного осаждения смеси гелеобразующих растворов жидкого стекла и подкисленного сернокислого алюминия в минеральном масле. Он весьма активен (индекс активности 37— 39%) 1 успешно используется в каталитическом крекинге с подвижным слоем катализатора. Слой шариков в реакторе оказывает меньшее сопротивление проходу паров, что обусловливает меньшие [c.81]
Раствор жидкого стекла вливается в смеситель с большой скоростью в струю раствора сернокислого алюминия и завихряет поток, благодаря чему растворы смешиваются практически мгновенно. Образующийся при смешении растворов золь из смесителя по трубке успокоителя потока спокойной струей поступает на вершину формующего конуса, распределяется на 72 струйки и стекает в турбинное масло в формовочную колонну. Потеряв в слое масла скорость, образовавшиеся шарики продолжают медленно опускаться вниз по колонне, попадают в формовочную воду и ее потоком по выносной трубе поднимаются в транспортный желоб. Выносная труба выведена почти на верх колонны, чтобы уровновесить уровень масла в колонне и водной взвеси шариков в трубе. Высота трубы определяет уровень раздела масла и воды в колонне и регулируется наставными кольцами. По желобу шарики водой транспортируются в промывочный чан, в котором они остаются, а вода по сливному шлангу через воронку и трубопроводу самотеком возвращается в промежуточную емкость, откуда насосом направляется в формовочные колонны. [c.84]
Физическая и коллоидная химия (1988) — [ c.165 ]
Общая химия в формулах, определениях, схемах (1996) — [ c.115 ]
Общая и неорганическая химия Изд.3 (1998) — [ c.142 ]
Общая химия в формулах, определениях, схемах (0) — [ c.5 , c.115 ]
Общая химия в формулах, определениях, схемах (1985) — [ c.115 ]
Общая химия в формулах, определениях, схемах (0) — [ c.115 ]
Основы физико-химического анализа (1976) — [ c.77 , c.79 ]
Краткий курс физической химии Изд5 (1978) — [ c.292 , c.293 ]
Учебник физической химии (1952) — [ c.208 ]
Неорганическая химия (1950) — [ c.54 ]
Неорганическая химия (1969) — [ c.147 ]
Общая и неорганическая химия (1981) — [ c.127 ]
Курс физической химии Том 1 Издание 2 (1969) — [ c.0 ]
Курс физической химии Том 1 Издание 2 (копия) (1970) — [ c.0 ]
Учебник физической химии (0) — [ c.218 ]
Краткий курс физической химии Издание 3 (1963) — [ c.276 ]
Курс физической химии Издание 3 (1975) — [ c.350 ]
Общая химия Биофизическая химия изд 4 (2003) — [ c.42 , c.43 ]
Химия Справочник (2000) — [ c.126 ]
chem21.info
Виды растворов. Виды концентрации растворов
Растворы – это состоящая из двух или более веществ однородная масса или смесь, в которой одно вещество выступает в качестве растворителя, а другое – в качестве растворяемых частиц.
Существует две теории трактовки происхождения растворов: химическая, основоположником которой является Менделеев Д. И., и физическая, предложенная немецким и швейцарским физиками Оствальдом и Аррениусом. Согласно трактовке Менделеева, компоненты растворителя и растворяемого веществ становятся участниками химической реакции с образованием неустойчивых соединений этих самых компонентов или частиц.
Физическая же теория отрицает химическое взаимодействие между молекулами растворяющего и растворяемого веществ, объясняя процесс образования растворов как равномерное распределение частиц (молекул, ионов) растворителя между частицами растворяемой субстанции вследствие физического явления, именуемого диффузией.
Классификация растворов по различным критериям
На сегодня нет единой системы классификации растворов, однако условно виды растворов можно сгруппировать по наиболее значимым критериям, а именно:
I) По агрегатному состоянию выделяют: твёрдые, газообразные и жидкие растворы.
II) По размерам частиц растворённого вещества: коллоидные и истинные.
III) По степени концентрации частиц растворённого вещества в растворе: насыщенные, ненасыщенные, концентрированные, разбавленные.
IV) По способности проводить электрический ток: электролиты и неэлектролиты.
V) По назначению и области применения: химические, медицинские, строительные, специальные растворы и др.
Виды растворов по агрегатному состоянию
Классификация растворов по агрегатному состоянию растворителя приводится в широком смысле значения этого термина. Принято считать растворами жидкие субстанции (причём в качестве растворяемого вещества может выступать как жидкий, так и твёрдый элемент), однако если учесть тот факт, что раствор – это гомогенная система из двух или нескольких веществ, то вполне логично признать также и твёрдые растворы, и газообразные. Твёрдыми растворами принято считать смеси, например, нескольких металлов, больше известных в обиходе как сплавы. Газообразные виды растворов – это смеси нескольких газов, пример – окружающий нас воздух, который представлен в виде соединения кислорода, азота и углекислого газа.
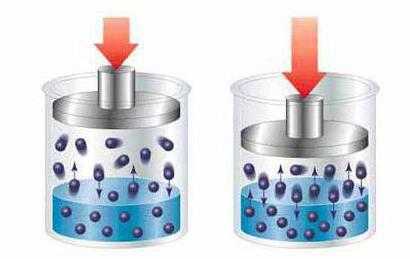
Растворы по размеру растворённых частиц
Виды растворов по размеру растворённых частиц включают истинные (обычные) растворы и коллоидные системы. В истинных растворах растворяемое вещество распадается на мелкие молекулы или атомы, по размерам приближённые к молекулам растворителя. При этом истинные виды растворов сохраняют первоначальные свойства растворителя, лишь слегка преображая его под действием физико-химических свойств добавленного в него элемента. Например: при растворении поваренной соли или сахара в воде вода остаётся в том же агрегатном состоянии и той же консистенции, практически такого же цвета, меняется только её вкус.

Коллоидные растворы отличаются от обычных тем, что добавляемый компонент распадается не полностью, сохраняя сложные молекулы и соединения, размеры которых значительно превышают частицы растворителя, превосходя значение 1 нанометра.
Виды концентрации растворов
В одно и то же количество растворителя можно добавить разное количество растворяемого элемента, на выходе будем иметь растворы с разной концентрацией. Перечислим основные из них:
- Насыщенные растворы характеризуются степенью растворимости вещества, при которой растворяемый компонент под влиянием постоянной величины температуры и давления больше не распадается на атомы и молекулы и раствор достигает фазового равновесия. Насыщенные растворы также условно можно разделить на концентрированные, в которых массовая доля растворённого компонента сопоставима с растворителем, и на разбавленные, где растворённого вещества в несколько раз меньше растворителя.
- Ненасыщенные – это те растворы, в которых растворяемое вещество ещё может распадаться на мелкие частицы.
- Пересыщенные растворы получаются тогда, когда изменяются параметры воздействующих факторов (температура, давление), в результате чего продолжается процесс «дробления» растворённого вещества, его становится больше, чем было при нормальных (обычных) условиях.
Электролиты и неэлектролиты
Некоторые вещества в растворах распадаются на ионы, способные проводить электрический ток. Такие гомогенные системы называются электролитами. В эту группу входят кислоты, большинство солей. А растворы, не проводящие электрический ток, принято называть неэлектролитами (почти все органические соединения).

Группы растворов по назначению
Растворы незаменимы во всех отраслях народного хозяйства, специфика которых создала такие виды специальных растворов, как медицинские, строительные, химические и другие.
Медицинские растворы – это совокупность препаратов в форме мазей, суспензий, микстур, растворов для инфузий и инъекций и прочих лекарственных форм, применяемых в медицинских целях для лечения и профилактики различных заболеваний.
Виды химических растворов включают в себя огромное множество гомогенных соединений, используемых в химических реакциях: кислоты, соли. Эти растворы могут быть органического или неорганического происхождения, водные (морская вода) или безводные (на основе бензола, ацетона и т. д.), жидкие (водка) или твёрдые (латунь). Они нашли своё применение в самых различных отраслях национального хозяйства: химическая, пищевая, текстильная промышленность.
Виды строительных растворов отличаются вязкой и густой консистенцией, из-за чего им больше подходит название смеси.
 Благодаря своей способности быстро затвердевать они с успехом применяются в качестве вяжущего материала для кладки стен, потолков, несущих конструкций, а также для отделочных работ. Представляют собой водные растворы, чаще всего трёхкомпонентные (растворитель, цемент различных маркировок, заполнитель), где в качестве наполнителя используется песок, глина, щебень, известь, гипс и другие строительные материалы.
Благодаря своей способности быстро затвердевать они с успехом применяются в качестве вяжущего материала для кладки стен, потолков, несущих конструкций, а также для отделочных работ. Представляют собой водные растворы, чаще всего трёхкомпонентные (растворитель, цемент различных маркировок, заполнитель), где в качестве наполнителя используется песок, глина, щебень, известь, гипс и другие строительные материалы.
fb.ru